Une bactérie qui s’attaque aux grands brûlés bientôt désarmée
Une étude de l’UNIGE dévoile les stratégies adoptées par une bactérie qui prolifère dans les plaies des grands brûlés et les menace de septicémie. Elle ouvre la voie à de nouvelles thérapies.
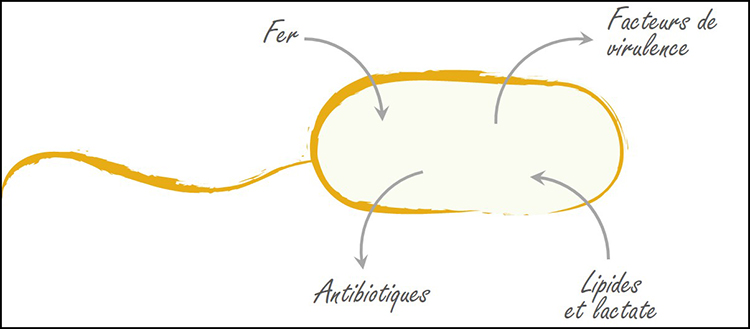
Vue d’ensemble des mécanismes mis en œuvre par Pseudomonas aeruginosa dans les exsudats de patients. (© UNIGE)
La bactérie Pseudomonas aeruginosa est l’une des causes principales d’infections et de septicémie chez les personnes souffrant de brûlures sévères, car elle est difficile, voire impossible, à combattre. Des chercheurs de l’Université de Genève (UNIGE) sont parvenus à révéler la dynamique de la physiologie et du métabolisme du pathogène au cours de sa croissance dans des exsudats, les liquides biologiques qui s’épanchent des plaies de personnes brûlées. Publiée dans la revue Frontiers in Cellular and Infection Microbiology, cette étude permet de suivre pas à pas les stratégies mises en place par Pseudomonas aeruginosa pour proliférer et, ainsi, de guider le développement de traitements innovants afin de les contrer.
Pseudomonas aeruginosa a été récemment classé par l’Organisation Mondiale de la Santé comme l’un des pathogènes prioritaires à cibler pour la mise au point de nouveaux traitements. Cette bactérie redoutable est responsable de divers types d’infections aiguës ou chroniques potentiellement létales. Les patients souffrant de brûlures sévères constituent un groupe à risque, car cet agent se développe dans les plaies et s’adapte à son environnement pour proliférer puis coloniser son hôte, pouvant ainsi provoquer une septicémie.
Ce micro-organisme, largement présent dans l’environnement, profite d’un affaiblissement de l’hôte pour mettre en place divers mécanismes qui facilitent sa multiplication. «Nous voulions savoir quelles armes étaient fabriquées et utilisées par P. aeruginosa et à quel moment au cours de l’infection. Nous avons donc identifié les gènes qui étaient exprimés par les bactéries mises en contact avec les exsudats de patients et s’y développant», explique Karl Perron, directeur du Laboratoire de bactériologie au Département de botanique et biologie végétale de la Faculté des sciences de l’UNIGE. L’analyse de l’expression des quelque 6’000 gènes bactériens a été couplée à celle des composés utilisés par P. aeruginosa, en collaboration avec des chercheurs du Centre hospitalier universitaire vaudois (CHUV) et de l’Hôpital universitaire de Berne.
Un pathogène mis à nu
«La bactérie surexprime très rapidement tous les gènes codant pour des protéines permettant de capter le fer de l’hôte, car il est nécessaire à sa croissance et à sa prolifération», détaille Manuel Gonzalez, membre de l’équipe genevoise et premier auteur de l’article. Il s’agit aussi bien de sidérophores, des molécules se liant au fer soluble, que d’hémophores, de véritables « aspirateurs moléculaires » extirpant le fer lié aux globules rouges. La bactérie fabrique aussi en parallèle divers systèmes permettant d’exporter et d’importer ces molécules, avant et après qu’elles aient capté le fer.
Les chercheurs ont également découvert que P. aeruginosa utilise essentiellement le lactate, les lipides et le collagène de l’hôte comme sources de nutriments. Afin d’accéder à ces composés, la bactérie produit et sécrète rapidement des enzymes spécifiques capables de détruire les tissus environnants.
Les biologistes ont montré que ces facteurs de virulence sont produits dans les exsudats même lorsque ceux-ci ne contiennent que relativement peu de P. aeruginosa, suggérant que ce pathogène devient rapidement agressif dans les plaies de brûlure. «Nous avons également observé qu’il génère des pompes servant à expulser des molécules, ce qui pourrait lui permettre de résister à certains antibiotiques», ajoute Karl Perron.
Introduire un cheval de Troie dans la colonie
Ces résultats, qui révèlent la dynamique de la physiologie et du métabolisme de P. aeruginosa dans un contexte de brûlure, fournissent des éléments cruciaux pour élaborer de nouvelles approches thérapeutiques. «Etant donné que la disponibilité en fer est un facteur limitant pour la croissance bactérienne, il faut envisager une stratégie du type ‘cheval de Troie’, qui est en cours de développement. Cela consiste à lier certains antibiotiques à des sidérophores pour que la bactérie les importe en grandes quantités, en même temps que le fer soluble», expose Manuel Gonzalez. Des molécules inhibant des facteurs de virulences spécifiques pourraient aussi être administrées de façon précoce.
Pour cette recherche, les microbiologistes ont eu recours à une méthode alternative à l’expérimentation animale. L’analyse des exsudats, leur utilisation et la synthèse d’un milieu artificiel mimant cet environnement particulier ont valu à Karl Perron le ‘Prix 3R 2017 de l’UNIGE’. La règle des 3R (reduce, replace, refine) s’est imposée internationalement comme le fondement de la démarche éthique appliquée à l’expérimentation animale, et est activement promue par l’UNIGE. Elle pousse à réduire le nombre d’animaux utilisés, à raffiner les conditions expérimentales pour améliorer le bien-être animal, et à remplacer le modèle animal par d’autres méthodes expérimentales lorsque cela est possible.
