Première partie
1. Introduction
1.1 Considérations générales
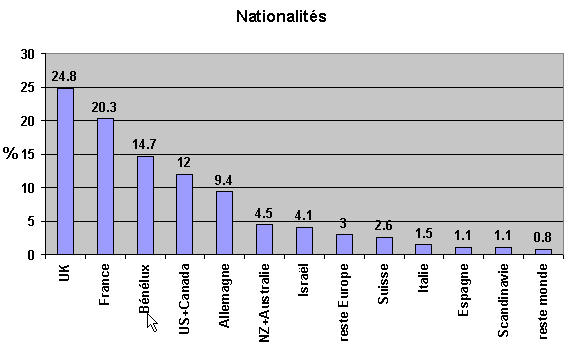
De nos jours, la marche en haute et très haute montagne 1 n'est plus seulement une affaire de spécialistes. En effet, la société occidentale, suite à un développement économique sans précédent, offre aujourd'hui à une grande partie de sa population un large accès aux loisirs, notamment dans les domaines sportif et touristique. Parmi les citadins, toujours plus nombreux, on observe souvent ce désir de retrouver le contact avec le milieu naturel, au moins pour le temps des vacances, désir parfois associé à une recherche d'exotisme. Les régions himalayennes présentent, à ce point de vue, de nombreux atouts : vastes régions montagneuses, aux paysages d'une grande diversité et d'une exceptionnelle beauté, qu'on ne peut rejoindre qu'à pied ou à dos de mulet (aspect 'nature'), associées à un dépaysement garanti, lié au fait que la culture asiatique est fort différente de la culture occidentale (aspect 'exotisme'). Le Népal accueillerait chaque année plus de 60'000 randonneurs en provenance des pays occidentaux 59. En 1997, 8'000 Suisses se sont rendus au Népal (ils étaient 7'300 en 1996 et 6'200 en 1995) 2 .
La pathologie de haute altitude touche donc de plus en plus de monde et l'effort fait pour améliorer la diffusion de l'information sur les dangers de la montagne, au cours des dernières décennies, mérite d'être poursuivi. En effet, le mal d'altitude ou mal aigu des montagnes (MAM) peut affecter toute personne qui monte à plus de 2'500 mètres d'altitude. La baisse de la pression partielle d'oxygène dans l'air, d'autant plus importante que l'altitude atteinte est élevée, est à l'origine de cette pathologie. Celle-ci est, dans la plupart des cas, bénigne et spontanément régressive, mais peut parfois évoluer vers l'oedème cérébral de haute altitude (OCHA), potentiellement mortel.
Ce travail constitue l'un des volets d'une étude menée en octobre 1998. L'autre volet de l'étude, effectué par le Dr Samuel Gaillard, consistait à comparer nos résultats avec ceux de l'étude réalisée par le Dr Bengt Kayser, en 1986, dans les mêmes
conditions 28. M. Gaillard a entre autres cherché à mettre en évidence une modification du comportement des marcheurs en faveur d'une meilleure acclimatation, suite à une plus large diffusion de l'information sur le MAM au cours de cette dernière décennie.
Dans ce travail, un nouveau questionnaire d'évaluation du MAM dit 'de Lake Louise' a été comparé à l''Environmental Symptoms Questionnaire' ('ESQ') 55, déjà reconnu comme fiable et utilisé jusqu'alors dans la plupart des enquêtes épidémiologiques sur le mal aigu des montagnes, afin vérifier la validité du premier en milieu himalayen. En effet, la comparaison de ces deux questionnaires a déjà été faite dans les Alpes 5, mais pas encore dans l'Himalaya, où la vitesse de progression et les altitudes atteintes diffèrent notablement.
1.2 Plan de l'ouvrage
Quelques lignes sur la physique atmosphérique concluent cette introduction. Le chapitre suivant nous familiarise avec divers historiens, missionnaires ou savants qui furent eux-mêmes victimes du MAM ou dont les découvertes firent progresser la compréhension de cette pathologie. Un exposé sur les connaissances actuelles du MAM suit et enfin, un compte-rendu de la méthode utilisée pour réaliser notre étude clôt la première partie.
La seconde partie expose les résultats de l'étude : tout d'abord, les caractéristiques de la population étudiée puis, les corrélations existant entre les deux types de questionnaires et enfin, les corrélations entre les différentes caractéristiques de la population et la prévalence du MAM, afin de mettre en évidence d'éventuels facteurs de risque. Une discussion sur les résultats de l'étude et les conclusions qui en découlent terminent cet ouvrage.
1.3 Quelques notions de physique 3
L'oxygène constitue 21% des gaz atmosphériques, quelle que soit la valeur de la pression barométrique (qui correspond au poids de l'atmosphère). Comme celle-ci diminue avec l'altitude, il en va de même pour la pression partielle d'oxygène. La pression barométrique vaut environ 760mmHg au niveau de la mer et environ 253mmHg au sommet de l'Everest (8'850 mètres d'altitude). La pression partielle d'oxygène est alors respectivement de 159mmHg et de 53mmHg dans l'air et de 105mmHg (14kPa) et d'environ 33mmHg (4,4kPa) dans le sang artériel, au repos. Ces valeurs, rencontrées en altitude extrême, ne sont tolérées que par les organismes acclimatés, c'est-à-dire dont la montée en altitude a été progressive (sur plusieurs semaines, voire plusieurs mois pour ce qui est de l'Everest). En effet, si une telle hypoxémie survient de façon aiguë, elle est le plus souvent létale.
Cependant, la pression barométrique ne diminue pas de façon linéaire avec l'altitude : si la température était constante, la chute de pression se ferait de manière exponentielle, en raison du poids de l'atmosphère supérieure qui comprime les gaz atmosphériques inférieurs. Mais parce que la température diminue avec l'altitude (d'environ 1°C tous les 150 mètres), indépendamment de la latitude, la pression baisse plus rapidement que ne le prédisent les lois exponentielles (en 1906, Nathan Zuntz, physiologiste allemand, a démontré qu'une élévation de la température ambiante augmente la pression barométrique et inversement). La pression barométrique varie donc également avec les saisons : l'hiver est ainsi une saison peu propice à l'escalade des hauts sommets, car non seulement le froid y est plus intense, mais en plus celui-ci entraîne une chute plus importante de la pression partielle d'oxygène de l'air.
L'atmosphère est divisée en trois couches sur la base de la température :
- la troposphère, dans laquelle se déroulent les phénomènes météorologiques et où la température décroît de manière linéaire jusqu'à - 60°C, s'étend du niveau de la mer jusqu'à 9'000 mètres d'altitude aux pôles et jusqu'à 19'000 mètres à l'équateur.
- la stratosphère, au-delà de la troposphère, s'étend sur 10 à 12 kilomètres 'd'épaisseur' ; la température y est constante (- 60°C).
- la région atmosphérique qui surplombe ces deux zones renferme notamment la ionosphère qui permet la transmission des ondes radiophoniques.
Il apparaît donc que la troposphère est plus 'épaisse' au niveau de l'équateur et qu'elle s'amincit au fur et à mesure qu'on se rapproche des pôles. Car il y a dans la stratosphère située au-dessus de l'équateur une masse très importante d'air froid qui 'pèse' sur la troposphère sous-jacente. Ainsi, la pression barométrique varie également en fonction de la latitude : la pression partielle d'oxygène est plus importante sur un sommet de 6'000 mètres d'altitude proche de l'équateur que sur un sommet de même altitude plus éloigné de la latitude équatoriale. L'Everest est donc situé à une latitude favorable à son escalade et, s'il était plus éloigné de l'équateur, il serait probablement impossible d'atteindre son sommet sans apport artificiel d'oxygène. En effet, il semble que la pression partielle d'oxygène au sommet de l'Everest correspond à l'hypoxie maximale qui peut être tolérée par l'organisme humain.
Le froid est, avec l'hypoxie, le facteur de stress le plus important rencontré en altitude. Pour refroidir l'organisme, la présence ou l'absence de vent joue un rôle plus déterminant que la température elle-même. On peut rencontrer des vents allant jusqu'à 200km/h au sommet du Mont-Blanc et jusqu'à 300km/h sur l'Everest.
L'humidité absolue de l'atmosphère (quantité de vapeur d'eau par unité de volume de gaz) diminue avec la température. Ainsi, en altitude, même si l'air est saturé en vapeur d'eau, l'humidité effective est très basse. Cette sécheresse de l'air favorise la déshydratation de l'organisme en amplifiant les pertes insensibles, via la transpiration et la respiration. De plus, l'augmentation de la fréquence respiratoire, en réaction à l'hypoxie d'altitude et à l'effort, contribue également à accentuer ces pertes. Au-delà de 6'000 mètres, il convient d'absorber trois à quatre litres de liquide par jour pour pouvoir maintenir une diurèse d'un litre et demi par jour.
2. Historique
Le texte le plus ancien évoquant le mal des montagnes qui nous soit parvenu remonte à 30 ans avant Jésus-Christ ! Il est dû à un historien chinois qui décrit le mal étrange auxquels étaient confrontés ceux qui cheminaient dans les hauteurs himalayennes. Au XVIe siècle, les Espagnols, au cours de leur conquête de l'Amérique, se rendent parfois dans les Andes, où, là aussi, certains succombent à cette pathologie d'altitude. Aux XVIIe et XVIIIe siècles, plusieurs savants (notamment Pascal, Boyle, Lavoisier) font d'importantes découvertes concernant les lois physiques et chimiques de l'atmosphère. Les découvertes scientifiques se poursuivent au XIXe siècle, notamment dans le domaine de la physiologie d'altitude avec le français Paul Bert et l'italien Angelo Mosso. C'est aussi le siècle où l'alpinisme prend son essor, notamment avec la fondation du premier club alpin en Grande-Bretagne. Au XXe siècle enfin, la recherche en physiologie et physiopathologie de l'altitude est en pleine expansion : dans ce but, un nombre impressionnant d'expéditions sont organisées, sur tous les continents ; on installe parfois des laboratoires d'altitude. La recherche s'effectue également en laboratoire au niveau de la mer, grâce aux chambres de décompression. On met en évidence que l'hypoxie joue un rôle crucial dans le développement du mal aigu des montagnes, mais que ce n'est cependant pas le seul facteur en cause : en effet, comment se fait-il que certaines personnes soient atteintes par ce mal et d'autres pas ? Pourquoi une personne qui n'a jamais présenté de problèmes en altitude, développera-t-elle un jour un oedème cérébral de haute altitude ? Aujourd'hui encore ces questions sont débattues.
Environ 30 ans avant Jésus-Christ : sous le règne de l'empereur chinois Ching-Te (32-7 avant J.-C.), Tseen Han Shoo, dans son histoire classique de la Chine, mentionne les montagnes du grand mal de tête et du petit mal de tête, sur la route qui va des régions de l'ouest de la Chine à l'Hindu Kush (Afghanistan). Il écrit : 'Lorsque les hommes passent par la montagne du grand mal de tête et celle du petit mal de tête, par le pays rouge et par la pente de la fièvre, leur corps devient fiévreux et livide et ils sont en proie à des maux de tête et à des vomissements ; les ânes et le bétail sont dans le même état. (...) Les hommes perdent leur faculté de compréhension et ne sont plus à même de s'entraider.' 4
403 : le chinois Fa-Hsien, voyageant au Cachemire et en Afghanistan, rapporte qu'alors qu'il gravissait une montagne avec son compagnon, ce dernier a commencé à être de plus en plus faible, à avoir la bouche pleine d'écume et un état de conscience fluctuant. Il est finalement mort au cours de l'ascension.
1519 : Hernán Cortés, conquistador espagnol au Mexique, envoie Diego Ordaz faire l'ascension du mont Popocatepetl (volcan du Mexique, culminant à 5'452 mètres). Ce dernier rapporte : 'Pour accroître encore la difficulté, la respiration dans ces hauteurs devient si difficile que chaque effort s'accompagne d'une vive douleur dans la tête et dans les membres.'
1531 : les Mongols envahissent le Ladakh et l'ouest du Tibet. Ils décrivent les symptômes du MAM qu'ils appellent yas : vomissements, épuisement, troubles du sommeil et gonflement des mains et des pieds. Ils notent qu'alors la mort survient souvent, si la descente n'est pas rapide. Les Tibétains l'appellent damgiri (crise respiratoire) ou dugri (poison de la montagne).
1590 : José de Acosta, prêtre jésuite ayant accompagné les conquistadores espagnols au Pérou, publie à Séville son Histoire naturelle et morale des Indes de l'est et de l'ouest. Cet ouvrage comprend l'un des premiers récits détaillés sur le MAM : 'Il y a, au Pérou, une haute montagne appelée Pariacaca. Ayant entendu parlé des troubles physiques qui y survenaient, je m'y rendis aussi bien préparé que je pus, selon les instructions qui m'avaient été données par ceux qu'on appelle les vagutanos, c'est à dire des hommes expérimentés. Mais, malgré toutes mes précautions, quand je parvins en haut de ce qu'ils appellent les 'degrés' b 5 , je fus soudain pris d'une telle sensation, à la fois bizarre et terrible, que j'étais prêt à m'écrouler par terre. Et bien que nous fûmes nombreux dans le groupe, chacun se dépêchait, sans attendre son compagnon, pour s'échapper rapidement de cette mauvaise passe. Me retrouvant seul avec un Indien, que je suppliais de m'aider à me relever, je fus en proie à de telles douleurs étreignantes et à de tels hauts-le-coeur que je crus que j'allais vomir aussi mon propre coeur ; car j'avais déjà vomi mon repas, de la lymphe et de la bile (la jaune et la verte) ; finalement, je vomis aussi du sang tout en ayant des crampes d'estomac. Pour conclure, je serais indubitablement mort, si cela avait continué ; mais, après trois ou quatre heures, nous arrivâmes dans un endroit plus agréable et plus conforme à notre nature, où je trouvai tous mes compagnons (au nombre de quatorze ou quinze) complètement épuisés. Certains, au cours de ce passage, demandèrent la confession, pensant vraiment mourir ; d'autres sortirent du chemin, terrassés par des vomissements et devant aller à selles. On m'a dit que des hommes avaient déjà perdu la vie suite à ces troubles. J'en ai vu un qui se projetait contre le sol en pleurant de rage et de douleur à cause de ce que ce passage par Pariacaca avait provoqué. Mais le plus souvent cela ne causait pas de gros dommages, seulement cette douleur et un certain dégoût pendant qu'on l'endure. Et il n'y a pas que le passage de Pariacaca qui a cette propriété, mais aussi toutes les arêtes des montagnes qui passent à plus de cinq cents lieues (...).' Il écrit également : 'C'est pourquoi je suis persuadé que l'air qui y est trop subtile et délicat n'est pas adapté à la respiration humaine qui a besoin d'un air plus grossier et plus tempéré.' 6
Le MAM est appelé puna en Bolivie, soroche au Pérou ou encore mareo ou veta.
1624 : le père jésuite portugais Antonio Andrada est le premier Européen à entrer au Tibet. Il pense que le mal des montagnes est essentiellement causé par le froid.
1648 : Blaise Pascal démontre que la pression atmosphérique diminue avec l'altitude.
1660 : sir Robert Boyle, physicien, chimiste et philosophe irlandais, publie ses Nouvelles expériences physiques et mécaniques sur la qualité de l'air et ses effets 7 .
Il écrit notamment : '(...) comme le relate Aristote, ceux qui montaient au sommet du mont Olympe (2'917m) ne pouvaient rester en vie à moins de prendre avec eux des éponges humidifiées, grâce auxquelles ils pouvaient respirer cet air, trop fin pour la respiration.' En 1978, Kellogg, malgré ses recherches, n'a pas pu retrouver ce passage d'Aristote, qui avait aussi été cité par beaucoup d'autres. Il a pensé qu'il s'agissait plutôt d'un passage de Saint Augustin (354-430) qui parle des effets de la faible humidité en altitude.
1661 : les pères Grüber et D'Orville, jésuites, quittent Pékin et rejoignent Katmandou en passant par le Thung La. Le père Grüber dit, en parlant de l'Himalaya : 'On ne peut y respirer parce que l'air y est trop subtil.' Il pense que le mal des montagnes est aussi causé par la mauvaise odeur de plantes empoisonnées qui poussent à ces altitudes.
1716 : le père Desiderei, fondateur d'une mission à Lhassa et qui souffrait d'importantes céphalées, pense que le MAM est dû à certains matériaux présents en altitude et qui empestent l'air, mais aussi au fait que celui-ci est vif et fin.
1777 : Antoine Laurent de Lavoisier, chimiste parisien, découvre la nature de l'oxygène et décrit son rôle dans la combustion et dans la respiration des êtres vivants.
1786 : Jacques Balmat, chamoniard, est le premier à atteindre le sommet du Mont Blanc (4'807m) avec deux compagnons, dont le Docteur Michel-Gabriel Paccard. Ils attribuent les malaises ressentis au cours de l'ascension 'à la chaleur et à la stagnation de l'air'.
1787 : c'est au tour d'Horace-Bénédict De Saussure, géologue et physicien genevois, d'atteindre le plus haut sommet des Alpes. Il écrit : 'J'ai souvent conduit avec moi des paysans, d'ailleurs très robustes, qui, à une certaine hauteur, se trouvaient tout à coup incommodés, au point de ne pouvoir absolument monter plus haut ; et ni le repos, ni les cordiaux, ni le désir le plus vif d'atteindre la cime de la montagne ne pouvaient leur faire passer cette limite. Ils étaient saisis, les uns de palpitations, d'autres de vomissements, d'autres de défaillances, d'autres d'une violente fièvre, et tous ces accidents disparaissaient au moment où ils respiraient un air plus dense.' 8 Au cours de sa troisième ascension, De Saussure présente une fatigue très intense, dont on pensait à l'époque qu'elle était à l'origine du mal des montagnes : 'Quand je commençai cette ascension, je manquais passablement de souffle à cause de la rareté de l'air... Le genre de fatigue qui résulte de la rareté de l'air est insurmontable et quand elle survient à une telle altitude, même si le plus terrible des dangers survenait, vous ne pourriez pas faire un pas de plus.' Proche du sommet, il se plaint d'un épuisement extrême : 'Ce besoin de me reposer était absolument insurmontable ; si j'avais essayé de le surmonter, mes jambes auraient refusé de bouger, j'étais proche de l'évanouissement et j'étais en proie à des vertiges...'. Une fois arrivé au sommet, il écrit : 'Quand j'avais à faire un effort pour disposer mes instruments et faire des observations, j'étais constamment contraint d'interrompre mon travail pour me consacrer uniquement à respirer.' 9 De Saussure pense que l'air au sommet du Mont Blanc est moins dense à cause de son contact étroit avec la neige.
1802 : le savant et voyageur berlinois Alexander von Humboldt gravit le Mont Chimborazo (5'600m), en Equateur. Il décrit dans son ouvrage Voyage aux régions équinoxiales du Nouveau Continent la survenue, au cours de l'ascension, de malaises et de nausées, accompagnés d'un saignement des lèvres et des gencives. Il pense qu'en altitude, la pression barométrique n'est plus suffisante pour maintenir la tête fémorale dans la cavité cotyloïde, travail qui doit alors être effectué par les muscles qui, de fait, se fatiguent plus vite.
1852 : Radhanath Sikhdar, calculateur bengali dépendant du Bureau topographique de Calcutta, découvre que l'Everest (appelé alors 'pic XV' par les Occidentaux, 'Chomolungma', c'est-à-dire 'déesse mère du monde' par les Tibétains et 'Sagarmatha', 'déesse du ciel' par les Népalais) est le plus haut sommet du monde. D'après ses calculs trigonométriques, il atteint 8'839 mètres d'altitude 10 .
1855 : Hermann et Robert Von Schlagintweit, voyageurs allemands, montent à presque 7'000 mètres sur le Mont Ibi Gamin, dans le Garwhal Himal (Inde).
1857 : fondation du premier Club Alpin en Grande-Bretagne. Première escalade du Mont Blanc du physicien irlandais John Tyndall. Son compagnon constate que la respiration périodique nocturne est particulièrement marquée en altitude : 'Vous m'avez presque effrayé : j'ai écouté pendant quelques minutes et je ne vous ai pas entendu respirer une seule fois.' 11
1865 : sir Andrew Waugh, arpenteur général des Indes, attribue au pic XV le nom de 'Mont Everest' en l'honneur de sir George Everest, son prédécesseur.
1878 : Paul Bert, élève de Claude Bernard, publie La pression barométrique 12 , considéré comme le premier ouvrage de référence sur les effets de la diminution de la pression atmosphérique sur l'organisme. Il est le premier à conduire des expériences en chambre de décompression et à mettre clairement en évidence que la cause véritable du mal des montagnes est la baisse de la pression partielle d'oxygène. Il parvient, en extrapolant à partir des mesures faites dans les Andes, en 1875, par le Dr Jourdanet, à déterminer la pression barométrique au sommet de l'Everest qu'il fixe à 248mmHg. 13
1879 : l'alpiniste anglais Edward Whymper, vainqueur du Cervin en 1865, monte une expédition dans les Andes pour étudier le MAM. Il divise les signes cliniques en 'permanents' (notamment perte d'appétit, fatigue, augmentation de la fréquence respiratoire) et 'transitoires' (augmentation de la tension artérielle, de la température corporelle et de la fréquence cardiaque).
1890 : F. Viault constate, également par des études menées dans les Andes, que l'érythropoïèse est stimulée par l'altitude.
1891 : Rockhill relève que le MAM est appelé yen-chang au Koko Nor et chang chi au Szechuan, les deux expressions signifiant 'vapeurs pestilentielles' (dont on pensait qu'elles émanaient de la grande quantité de rhubarbe poussant à ces altitudes). L'ail et le tabac étaient considérés comme des antidotes par les indigènes. Quant aux Tibétains, ils considéraient que, pour remédier au mal des montagnes, il fallait inciser le front à la racine des cheveux !
1894 : Egli-Sinclair écrit dans un article sur le MAM : 'La respiration est du même type que la respiration de Stokes, c'est-à-dire qu'elle paraît régulière pendant un certain temps, puis apparaissent quelques cycles respiratoires profonds et rapides, suivis d'un arrêt complet de la respiration pendant quelques secondes.' Il se réfère à la description rapportée, en 1854, par le médecin irlandais William Stokes : 'Ce type de respiration consiste en la survenue de séries d'inspirations augmentant progressivement jusqu'à un maximum, puis déclinant en intensité et en durée jusqu'à ce que s'établisse un état apparent d'apnée'. Un autre médecin irlandais du nom de John Cheyne avait déjà décrit ce type de respiration en 1818 ; on l'appela donc respiration 'de Cheyne-Stokes'.
1898 : Angelo Mosso, professeur de physiologie à Turin, entreprend la construction du laboratoire d'altitude de la 'Capanna Regina Margherita', au sommet du Mont Rose (4'553m). Il pense que le MAM est dû à la baisse de la pression partielle de CO2 dans le sang plutôt qu'au manque d'oxygène. Il est le premier à effectuer, en altitude, le relevé de tracés de la respiration périodique nocturne. Dans son livre Vie d'un homme dans les Hautes Alpes, il fait une description clinique complète d'un cas fatal d'oedème pulmonaire de haute altitude, comprenant également le rapport d'autopsie (il s'agit du cas du Dr Jacottet, médecin à Chamonix, mort en 1891, à 4'300 mètres, lors d'une ascension du Mont Blanc). L'autopsie mit en évidence un coeur normal et un oedème pulmonaire. On posa le diagnostic post mortem de pneumonie. En effet, on pensait que les poumons se remplissaient d'eau à la suite d'une infection.
1901 : le Dr Malcolm Hepburn publie une revue sur les théories du MAM des XVIIIe et XIXe siècles dans laquelle il conclut : 'Il nous faut encore prouver que la dyspnée et la fatigue sont dues au manque d'oxygène, même si les probabilités vont dans ce sens.'
1909 : le duc des Abruzzes, aristocrate italien, tente l'ascension du K2 (8'811m), dans les montagnes du Karakoram, à la frontière du Pakistan et de la Chine. Sans atteindre le sommet, l'expédition parvient toutefois à 7'500 mètres, sans apport artificiel d'oxygène. C'est aussi l'année de la conquête du Pôle Nord par l'explorateur américain Robert Peary.
1910 : le physiologiste anglais Joseph Barcroft conduit la 'First International High Altitude Expedition' à la cabane Alta Vista (3'350m), sur le Mont Tenerife, dans les îles Canaries. Il démontre que l'hypoxie est à l'origine du mal des montagnes et non pas l'hypocapnie, comme le croyait Mosso.
1911 : conquête du Pôle Sud par Roald Amundsen, norvégien. Dès lors l'Everest reste le 'troisième pôle', le plus convoité des explorateurs terrestres. Depuis la découverte de Sikhdar, en 1852, et jusqu'à ce que le sommet soit atteint pour la première fois, en 1953, quinze expéditions se succédèrent et vingt-quatre hommes y perdirent la vie.
1913 : T. Ravenhill, médecin dans un district minier du Chili, à environ 4'800 mètres d'altitude, est le premier à effectuer une classification des symptômes et des signes du MAM. Il publie Quelques expériences du mal des montagnes dans les Andes 14 . Il décrit la puna de types 'normal, cardiaque ou nerveux'. Voici sa description du type 'normal' : 'C'est un fait curieux que les symptômes de la puna ne se manifestent pas d'emblée. La majorité des nouveaux venus disent qu'ils se sentent bien lors de leur arrivée en altitude. C'est en général vers le soir que le patient commence à se sentir faible et peu enclin à l'effort. Il présente parfois des vomissements et, fréquemment, une sensation d'oppression thoracique. Plus rarement, il peut y avoir une détresse respiratoire ou une modification de la fréquence respiratoire normale tandis que le patient est au repos. Lorsqu'il se lève du lit, il peut être un peu étourdi et toute tentative d'effort augmente la céphalée, qui est presque toujours de localisation frontale.' Les types cardiaque et nerveux que décrit Ravenhill correspondent respectivement à l'oedème pulmonaire de haute altitude (OPHA) et à l'oedème cérébral de haute altitude (OCHA). Il pensait que l'oedème pulmonaire survenait suite à une défaillance cardiaque par manque d'oxygène, bien qu'il se fût agi de jeunes patients en bonne santé, comme il l'observait lui-même. Il constata d'ailleurs que certaines personnes souffrant de problèmes cardiaques ne développaient pas forcément un OPHA en se rendant en altitude.
1919 : Alexander M. Kellas, physiologiste et professeur de chimie à Londres, participa à huit expéditions dans l'Himalaya. Il écrit cette année-là Considération sur la possibilité d'escalader le Mont Everest 15 . Il est le premier physiologiste à analyser sérieusement les facteurs limitant l'effort physique en altitude extrême.
1920 : Joseph Barcroft publie les résultats d'une étude faite sur lui-même, pendant qu'il passait six jours en chambre de décompression. En 1925, il publie Leçons de haute altitude 16 , où il démontre notamment que l'oxygène n'est pas sécrété par les poumons, mais qu'il diffuse à travers eux.
1921 : le gouvernement tibétain ouvre ses frontières aux étrangers. Les premières expéditions sur l'Everest (les huit premières furent anglaises) se font donc sur la face nord de la montagne. La même année, Kellas, dans son manuscrit Le processus d'acclimatation à l'altitude 17 , émet de nombreuses hypothèses qui seront vérifiées après sa mort.
1924 : Edward Felix Norton participe à la troisième expédition qui tente l'ascension de l'Everest. Les membres du groupe parviennent à 8'589 mètres, sans apport artificiel d'oxygène. Quatre jours après cette tentative, deux membres de l'expédition, George Leigh Mallory et Andrew Irvine, quittent le campement à l'aube pour tenter une nouvelle fois l'ascension. On ne les a jamais revus.
1925 : Carlos Monge 18 rapporte à l'Académie péruvienne de médecine un cas de polyglobulie chez un patient vivant à Cerro de Pasco (4'300m). On mit plus tard cette anomalie en relation avec le mal chronique des montagnes, auquel on a donné le nom de 'maladie de Monge'.
1927 : le Dr Crane, directeur de l'Hôpital Chulec à La Oroya (3'720m), au Pérou, rapporte des cas de patients atteints d'insuffisance cardiaque gauche sévère, ayant récupéré comme par enchantement, lors de leur descente en train sur Lima 27.
1935 : Edwards dirige l''International High Altitude Expedition', au Chili. Il constate qu'à l'effort, les lactates sanguins sont très bas chez les personnes acclimatées.
1937 : Alberto Hurtado (ayant exercé les mêmes fonctions que C. Monge) pense que l'oedème pulmonaire de haute altitude (OPHA) n'est pas dû à une infection, mais à l'altitude.
1946 : les médecins américains Charles Houston et Richard Riley mènent l''Operation Everest I'. Quatre recrues de la marine américaine restèrent trente-quatre jours en chambre de décompression. La pression fut diminuée jusqu'à 236mmHg, valeur dont on pensait alors qu'elle équivalait à celle du sommet de l'Everest (calculée à partir de valeurs standardisées de l'atmosphère, utilisées dans l'aviation). Les conclusions de cette étude furent notamment que l'homme peut survivre à l'altitude de l'Everest, que les sujets acclimatés résistent mieux aux très hautes altitudes et que la descente même rapide ne pose aucun problème (on craignait un arrêt respiratoire par perte du stimulus hypoxique) 26.
1948 : Monge publie Acclimatation dans les Andes, où il décrit les caractéristiques physiologiques et pathologiques engendrées par l'altitude, chez les populations andines.
1949 : le Népal ouvre ses frontières. Les physiologistes américains Hermann Rahn et Arthur Otis publient La réponse respiratoire de l'homme pendant et après l'acclimatation à la haute altitude 19 .
1950 : le nouveau gouvernement chinois communiste ferme les frontières du Tibet.
1952 : dans un laboratoire sous tente, au Menlung La (5'800m), près du Cho Oyu (8'153m), le médecin anglais Griffith Pugh met au point un système assez léger pouvant délivrer quatre litres d'oxygène par minute (deux fois plus que les appareils utilisés jusqu'alors). Cela permit d'une part d'accélérer la vitesse d'ascension des montagnards qui purent alors effectuer l'aller-retour entre le camp de base et le sommet pendant les heures du jour et d'autre part d'atténuer la déshydratation de l'organisme en freinant un peu l'augmentation de la fréquence respiratoire.
1953 : une équipe anglaise effectue la troisième tentative d'escalade de l'Everest depuis le Népal. Après deux mois d'effort, elle parvient à établir un camp rudimentaire à 8'503 mètres, sur l'arête sud-est. Le 29 mai, Edmund Hillary, néo-zélandais, et Tensing Norgay, népalais (sherpa), atteignent le sommet de l'Everest avec un apport artificiel d'oxygène. Les scientifiques doutaient encore à ce moment-là de la possibilité d'atteindre le sommet sans apport artificiel d'oxygène. De même, ils pensaient qu'une fois au sommet, respirer quelques minutes sans apport artificiel d'oxygène, devait entraîner une perte de connaissance. Néanmoins, arrivé à 8'848 mètres, Hillary enleva son masque pendant environ dix minutes : 'Je réalisai que je commençais à devenir maladroit avec mes mains et à me mouvoir très lentement. Alors je remis rapidement mon masque à oxygène et j'expérimentais une fois encore l'effet stimulant de seulement quelques litres d'oxygène'.
1960 : dans le cadre de l''Himalayan Scientific and Mountaineering Expedition', Pugh fait installer un laboratoire de physiologie, le 'Silver Hut', à 5'800 mètres, au pied de l'Ama Dablam (6'795m), dans la région de l'Everest. Il effectue des mesures de la consommation maximale d'oxygène (VO2max) à l'aide d'un vélo ergométrique sur un groupe de physiologistes ayant passé l'hiver à cette altitude et donc très bien acclimatés. Il montre que la VO2max diminue de manière exponentielle avec l'altitude pour arriver à une valeur de 20ml/kg/min au col de Makalu, à 7'440 mètres (pression barométrique de 300mmHg) 20 . Il prélève, à 7'830 mètres, des échantillons de gaz alvéolaire : la PAO2 est de 32,8mmHg et la PACO2 de 14,3mmHg. A l'effort, malgré l'augmentation de la PAO2, il observe une diminution de la saturation artérielle en O2 qu'il attribue à la limitation de la diffusion des gaz au niveau pulmonaire, limitation mise en évidence par la méthode de diffusion du monoxide de carbone. Il constate, au fil des mois passés à 5'800 mètres, malgré de relativement bonnes conditions de vie, une détérioration de l'organisme, se manifestant notamment par une diminution des capacités physiques et intellectuelles, ainsi que par une perte de poids. Il en conclut que l'organisme humain n'a pas les moyens de s'adapter pour vivre à une telle altitude. Il travaille notamment avec Michael Ward, James Milledge, Sukhamay Lahiri et John B.West.
1960 : Houston rapporte un cas d'OPHA dans le Colorado (Leadville, Colorado, se trouve à 3'100 mètres d'altitude). Il pense qu'il s'agit d'un cas de décompensation d'une insuffisance cardiaque latente, due à l'hypoxie associée à l'effort intense et au froid. La même année, un autre médecin américain, Herbert Hultgren exclut l'insuffisance cardiaque gauche comme étiologie de l'oedème pulmonaire de haute altitude, notamment à cause de l'absence de cardiomégalie, de souffle ou de
galop 27.
1962 : le Dr Hans Hecht, médecin à Salt Lake City, effectue le cathéterisme d'un patient souffrant d'OPHA, mettant ainsi en évidence les valeurs hémodynamiques propres à cette pathologie. La même année, ces données sont confirmées à l'Hôpital Chulec de La Oroya : une hypertension pulmonaire associée à une pression artérielle pulmonaire bloquée normale excluent formellement la possibilité d'insuffisance cardiaque gauche. L'inhalation d'oxygène qui entraîne une chute rapide de la pression artérielle pulmonaire indique la présence d'une vasoconstriction pulmonaire hypoxique 27.
1963 : Thomas Hornbein, médecin du Missouri, et Willi Unsoeld, professeur de théologie dans l'Oregon, atteignent le sommet de l'Everest par l'arête ouest empruntée pour la première fois et bien plus difficile que les deux autres voies empruntées jusqu'alors (l'arête sud-est et l'arête nord-est). A cause de cette difficulté, les alpinistes n'arrivèrent au sommet qu'à la tombée de la nuit et furent contraints d'y bivouaquer. Unsoeld eut des engelures profondes des orteils (pathologie qui n'est malheureusement pas rare en très haute montagne, même quand on ne bivouaque pas au sommet de l'Everest !).
1964 : la Chine envahit l'Inde et les soldats sont confrontés au mal aigu des montagnes et à l'oedème pulmonaire de haute altitude. Cela conduit les deux pays à s'intéresser davantage au sujet. Le même problème se pose lors du conflit entre l'Inde et le Pakistan dans le glacier Siachen du Karakoram.
1966 : Hultgren pense que le fait que la vasoconstriction hypoxique à travers le territoire pulmonaire n'est pas homogène est l'un des facteurs étiologiques les plus importants de l'OPHA 27.
1967 : installation d'un laboratoire permanent à 5'300'mètres sur le Mont Logan, en Alaska.
1973 : le physiologiste italien Paolo Cerretelli, au cours d'une expédition italienne sur l'Everest, observe qu'en altitude, la VO2max reste inférieure à celle du niveau de la mer même lorsque le sujet respire 100% d'O2. En effet, celle-ci ne dépassait pas 93% de la valeur du niveau de la mer. L'hypoxie d'altitude, qu'on faisait ainsi momentanément disparaître, n'apparaît donc plus comme le seul facteur limitant la VO2max. Parmi de nombreuses hypothèses, Cerretelli retient celle d'un mauvais captage périphérique de l'oxygène, suite à un déséquilibre du flux sanguin musculaire, peut-être consécutif à l'augmentation de la viscosité sanguine. La même année, ouverture d'un laboratoire permanent à Terskol, à environ 2'000 mètres d'altitude, au pied du Mont Elbruz (Caucase).
1978 : Reinhold Messner et Peter Habeler atteignent le sommet de l'Everest sans apport artificiel d'oxygène. Arrivé au sommet, Messner écrit : 'Voilà, je n'ai plus besoin de monter... Après ces heures d'un supplice à peine conscient, maintenant que j'ai échappé au rythme monotone de l'ascension et n'ai plus rien d'autre à faire qu'à respirer, un grand calme envahit mon corps. Comme si j'avais couru ma vie et savais que j'allais pouvoir me reposer pour toujours... L'esprit absent, je ne m'appartiens plus à moi-même, je ne suis qu'un poumon unique, étroit, haletant, qui plane au-dessus des cimes et des brouillards.' 21 Messner est, en 1980, le premier homme à gravir l'Everest en solitaire et, en 1986, il devient également le premier à avoir gravi les quatorze sommets de plus de 8'000 mètres, toujours sans apport artificiel d'oxygène.
1979 : Kobrick et Sampson réalisent un questionnaire, permettant de recueillir des données sur les symptômes qui peuvent survenir en altitude. Ils l'appellent 'Environmental Symptoms Questionnaire' ou 'ESQ'. Il comprend cinquante-deux questions auxquelles les marcheurs répondent quotidiennement au fur et à mesure de leur progression. A partir des réponses données, on calcule un score qui définit le degré de sévérité de telle ou telle pathologie, par exemple le mal des montagnes. L'année suivante, ils proposent une deuxième version ('ESQ-II'), comprenant cinquante-cinq questions et un système plus simple pour le calcul de score 54.
1981 : John B. West conduit l''American Medical Research Expedition to Everest'. Il effectue la première mesure de pression barométrique au sommet de l'Everest : 253mmHg. Christopher Pizzo y mesure la pression partielle des gaz alvéolaires : PAO2 de 36,5 à 38,7mmHg et PACO2 de 5,1 à 9mmHg, cette dernière mesure reflétant la tachypnée extrême. Les échantillons de sang prélevés au col sud
(7'925m) permettaient de prédire une alcalose extrême au sommet (pH estimé à 7,7).
1983 : Sampson propose une deuxième révision de l''Environmental Symptoms Questionnaire' ('ESQ-III') 55. Soixante-sept questions permettent d'évaluer non seulement les symptômes cérébraux et respiratoires qui peuvent être causés par l'altitude, mais aussi un large éventail de symptômes dus aux stress environnementaux (stress thermiques, effort physique, état d'éveil prolongé), ou encore à des affections indépendantes du milieu, telle une infection des voies respiratoires.
1985 : Houston conduit l'opération 'Everest II'. Huit volontaires passent quarante jours en chambre de décompression où la pression est diminuée graduellement jusqu'à 240mmHg. Il constate que la baisse de la pression barométrique entraîne une amélioration du rapport ventilation/perfusion à travers le territoire pulmonaire, mais aussi une augmentation de la résistance pulmonaire. La perte de poids survient notamment par manque d'appétit. Les valeurs de gaz artériels mesurés à l'effort révèlent une PaO2 de 26mmHg et une PaCO2 de 8-10mmHg ! L'Everest est probablement l'altitude maximale où l'homme peut se rendre sans apport artificiel d'oxygène 26.
1991 : le questionnaire 'ESQ-III', bien qu'il soit un outil fiable pour la recherche épidémiologique sur le MAM, est jugé insatisfaisant à cause du grand nombre de questions qu'il comporte. Au cours du septième symposium sur l'hypoxie, à Lake Louise, Canada, réunissant des spécialistes de l'altitude du monde entier, on adopte par consensus un nouveau questionnaire, dit 'de Lake Louise'. Il est simplifié par rapport à l'ESQ-III puisqu'il ne comprend que six questions. Il peut également être complété par un examen clinique ciblé, si un médecin se trouve sur place.
Printemps 1993 : quarantième anniversaire de la première ascension de l'Everest, quinze expéditions (294 personnes) tentent l'escalade.
Automne 1993 : le permis d'escalade de l'Everest, délivré par les autorités népalaises, vaut alors 50'000 $ pour une cordée de cinq personnes, plus 10'000 $ par personne supplémentaire, avec un maximum de sept participants. Il est en outre décidé que quatre expéditions par année seraient autorisées. Mais parce que la Chine ne demandait que 15'000 $ par grimpeur et n'en limitait pas le nombre, le flot des expéditions se dirigea vers le Tibet et des centaines de sherpas se retrouvèrent sans travail. Devant leur mécontentement, les autorités du Népal supprimèrent la restriction du nombre d'expéditions.
Entre 1921 et 1995 : plus de cent trente personnes sont mortes sur les flancs de l'Everest (environ un mort pour quatre alpinistes ayant atteint le sommet).
1996 : le Dr Urs Scherrer montre que l'inhalation d'oxyde nitreux dans l'OPHA diminue la pression artérielle pulmonaire, améliore l'oxygénation et déplace le flux sanguin pulmonaire vers la région qui n'est pas oedématiée.
1997 : l'équipe française de Jean-Paul Richalet réalise l'opération 'Everest III', à Marseille. Huit sujets vivent pendant un mois dans un caisson progressivement dépressurisé pour atteindre virtuellement le sommet de l'Everest.
1999 : Robert Roach, Charles Houston, Peter Hackett et Jean-Paul Richalet créent un site sur le réseau informatique d'Internet contenant plus de six mille références bibliographiques sur la physiologie et la médecine d'altitude 22 .
3. Symptômes et signes cliniques du mal aigu des montagnes
L'hypoxie d'altitude peut entraîner deux types d'affections aiguës :
- le mal aigu des montagnes (MAM), à proprement parler, correspond à une atteinte du système nerveux central. Il peut dégénérer en oedème cérébral de haute altitude (OCHA).
- l'oedème pulmonaire de haute altitude (OPHA) entraîne principalement des symptômes respiratoires.
Ces deux entités peuvent survenir ensemble ou séparément. Bien qu'elles soient toutes les deux causées par l'hypoxie d'altitude, elles sont actuellement considérées comme deux entités nosologiques différentes, car leurs mécanismes physiopathologiques diffèrent quelque peu 23 . Dans ce travail, nous parlerons essentiellement de la première entité.
3.1 Cinétique
Les symptômes apparaissent progressivement six à douze heures après l'arrivée en altitude et ont d'autant plus de risque de survenir que l'altitude atteinte est élevée et que la vitesse d'ascension a été rapide 3,17,19,33,47. En général bénins, ils disparaissent spontanément en 24 à 48 heures (au plus tard au cours du quatrième ou cinquième jour), si on reste à l'altitude à laquelle ils sont apparus. Ils ne réapparaissent plus à cette altitude, mais peuvent récidiver plus haut. S'ils persistent, il ne faut pas poursuivre l'ascension, car cela entraînerait inévitablement une aggravation des symptômes, voire une évolution vers un oedème cérébral ou un oedème pulmonaire, très invalidants et potentiellement mortels. Toutefois, il arrive que les symptômes empirent, même sans poursuite de l'ascension. Il faut alors redescendre sans tarder : une descente de seulement 500 mètres de dénivelé peut suffire à les faire disparaître (sinon, il faut continuer à descendre jusqu'à ce qu'ils aient disparu ou soient devenus très légers).
3.2 Facteurs de risque
Une personne ayant déjà été victime d'un MAM ou d'un OPHA a plus de risque de tomber à nouveau malade que quelqu'un qui n'a jamais souffert de l'altitude 25. Personne n'est néanmoins totalement à l'abri. En effet, la susceptibilité au mal des montagnes d'un individu peut varier dans le temps : on peut être monté de nombreuses fois à plus de 2'500 mètres sans n'avoir jamais présenté aucun symptôme et un beau jour, sans raison particulière, se retrouver dans l'impossibilité de continuer son ascension, terrassé par un mal de tête terrible ou par un oedème pulmonaire (ce phénomène est connu même des alpinistes les plus chevronnés). Certaines études semblent montrer que les jeunes sont plus souvent atteints de MAM 11,17,25. D'autres travaux mentionnent également comme facteurs de risque l'obésité ou le sexe féminin 25,28, mais ces derniers facteurs ne ressortent pas systématiquement. Selon d'autres études encore, une plus faible augmentation de la ventilation en réponse à l'hypoxie serait un facteur de risque 3,44,45,61. Mais là aussi toutes les études ne concordent pas ! En 1998, Roach 49 a effectué des observations chez des alpinistes en route pour le sommet du Mont McKinley (6'194m), en Alaska. Il constata, chez ceux qui présentaient une désaturation de l'oxyhémoglobine plus importante à 4'200 mètres, une plus forte incidence de MAM, lors de la poursuite de l'ascension. Chez tous ceux qui souffraient du MAM, le taux de saturation de l'oxyhémoglobine était inférieur à 84% (valeur prédictive positive de 100%), mais seulement 55% de ceux qui présentaient cette valeur n'étaient pas malades (valeur prédictive négative de 31%).
3.3 Le mal aigu des montagnes (MAM)
Le symptôme indispensable au diagnostic de mal aigu des montagnes est la céphalée. Il peut s'accompagner d'autres symptômes :
- des troubles du sommeil, allant d'une légère perturbation du sommeil à l'insomnie complète.
- des troubles digestifs, allant de la légère perte d'appétit à l'anorexie complète et/ou de discrètes nausées jusqu'aux vomissements. Il y a parfois une sensation de 'gueule de bois'.
- de la fatigue et une sensation de faiblesse qui peuvent aller jusqu'à la lassitude extrême, avec chute des performances physiques, irritabilité et désir d'isolement.
- des vertiges, une sensation d'étourdissement qui peuvent, à un stade avancé, évoluer vers une ataxie.
Les symptômes et signes révélant un MAM sévère sont les céphalées sévères, la lassitude extrême, avec irritabilité et désir d'isolement, l'ataxie et les vomissements. Ils en imposent pour une descente aussi immédiate que possible, car ils parlent pour un oedème cérébral débutant pouvant évoluer vers le coma et la mort. Si les symptômes ne sont pas très francs, il faut surveiller l'évolution du malade (une personne atteinte d'oedème cérébral perd peu à peu la capacité d'évaluer elle-même son état physique et mental).
Les signes cliniques qui peuvent accompagner les symptômes du MAM sont :
- des oedèmes sous-cutanés périphériques ayant une ou plusieurs localisations (mains, pieds et/ou visage). Ils se rencontrent aussi chez les personnes exemptes de symptômes, mais sont tout de même plus fréquents chez les malades (Hackett a trouvé, à 4'243 mètres d'altitude, une incidence de 18% chez les personnes bien portantes et de 64% chez celles qui souffraient de MAM). Ils seraient deux fois plus fréquents chez les femmes 16,19.
-
des troubles de l'état mental qui peuvent s'aggraver selon le schéma suivant :
- léthargie, lassitude
- désorientation, confusion
- stupeur, diminution de l'état de conscience
- coma
-
une ataxie (objectivée par une marche talon contre orteil ou un test de Romberg) pouvant être de plus en plus marquée :
- manoeuvres pour garder l'équilibre
- impossibilité de marcher sur une ligne droite
- chute
- impossibilité de se lever
- des râles pulmonaires discrets se rencontrent fréquemment en altitude, sans que la personne soit forcément malade. Néanmoins, comme dans le cas des oedèmes périphériques, ils se retrouvent davantage chez les malades : dans l'étude de Hackett, 23% de tous les sujets, malades ou non, en sont atteints à 4'243 mètres, contre 60% des sujets malades 19.
L'aggravation de ces signes avec apparition d'une ataxie, d'irrationalité, d'hallucinations et de nébulisation de la conscience sont fortement évocateurs d'un oedème cérébral de haute altitude : la descente doit être immédiate.
D'autres signes se rencontrent de façon plus sporadique : apparition d'une vision trouble due à une hémorragie rétinienne (elle-même sans gravité) ou à un oedème papillaire (compatible avec un OCHA). Les réflexes ostéo-tendineux peuvent devenir très vifs et le signe de Babinski peut devenir positif. Il peut y avoir une paralysie des muscles oculaires avec diplopie.
Au fur et à mesure que le MAM progresse, peuvent également survenir des symptômes et des signes d'oedème pulmonaire : une dyspnée qui s'accompagne souvent d'un pouls rapide et d'une cyanose. Les céphalées s'aggravent et l'ataxie devient telle que le patient ne peut même plus se tenir assis (ataxie tronculaire). Puis s'installe un coma et une respiration irrégulière. Sans traitement, la mort survient en quelques heures (au maximum en 48 heures).
3.4 L'oedème pulmonaire de haute altitude (OPHA)
Comme pour le MAM, l'OPHA est d'autant plus fréquent que l'altitude atteinte est élevée et que la vitesse d'ascension a été plus rapide 4,33 :
| Incidence de l'oedème pulmonaire de haute altitude (OPHA) | ||
| Altitude atteinte | Vitesse d'ascension | Incidence |
| 4'559m (Alpes) | 2 à 4 jours | 0,2% |
| 5'450m (Himalaya) | 6 jours | 2,3% |
| 4'559m (Alpes, pas d'antécédent d'OPHA) | 22 heures | 11% |
| 5'500m (Himalaya, soldats) | par avion | 15,5% |
| 4'559m (Alpes, avec antécédent d'OPHA) | 22 heures | 60% |
| Adapté de l'article de P. Bärtsch : Klinik und Pathophysiologie der Höhenkrankheit 4. | ||
Les patients qui souffrent de cette affection commencent par avoir une dyspnée d'effort plus marquée que celle des autres marcheurs. Elle s'accompagne souvent d'une fatigue inhabituelle et d'une toux sèche. Ils présentent des râles crépitants à l'auscultation pulmonaire, ainsi qu'une tachypnée et une tachycardie. L'apparition d'une dyspnée de repos signe l'aggravation des symptômes. Puis surviennent une cyanose et des expectorations mousseuses, parfois hémoptoïques. Le patient est le plus souvent subfébrile, mais il arrive que la température monte jusqu'à 39°C 4.Au stade de la dyspnée d'effort, il faut stopper l'ascension pour quelques jours. S'il n'y a pas d'amélioration après quelques jours de repos ou si les symptômes s'accentuent, la descente immédiate est impérative. L'oedème pulmonaire s'aggrave fréquemment pendant la nuit. Aux stades avancés de l'oedème pulmonaire apparaissent des symptômes d'OCHA.
3.5 Poser le diagnostic
3.5.1 MAM
Il y a plusieurs moyens de poser le diagnostic de MAM :
-
l'anamnèse du marcheur faite par un médecin et complétée par un examen clinique ciblé dans les heures qui suivent l'arrivée en altitude. Il existe plusieurs types de scores cliniques :
-
score de Hackett 17,19
Avec ce système de score, le médecin considère les point suivants : céphalées (valeur :1 point ou, si elles résistent aux analgésiques, 2 points), nausées ou anorexie (1 point), vomissements (2 points), insomnie (1 point), vertiges (1 point), oedème facial (1 point), dyspnée de repos (3 points), lassitude sévère (3 points) et ataxie (3 points). Le sujet est considéré comme atteint de MAM si son score est supérieur ou égal à 2 points. -
score de Maggiorini 5,37
Maggiorini reprend le score de Hackett, mais en le modifiant de la façon suivante : les items à 3 points sont supprimés, l'ataxie valant alors 2 points. Les oedèmes périphériques valent 1 point, s'ils n'ont qu'une localisation (mains, pieds ou visage) et 2 points, s'ils ont plus d'une localisation. La tachypnée et la dyspnée de repos valent 2 points et les râles pulmonaires 1 point, s'ils sont légers et 2 points, s'ils sont importants. Un score de 1 ou 2 correspond à un MAM léger et un score supérieur ou égal à 3 à un MAM sévère.
-
score de Hackett 17,19
Le score clinique est considéré comme l'étalon-or pour poser le diagnostic de MAM 37. Mais ce n'est pas un moyen très commode pour évaluer ce problème chez un grand nombre d'individus, étant donné qu'il exige la présence d'un médecin sur place.
-
Le système des questionnaires, distribués aux marcheurs et qu'ils remplissent eux-mêmes au fur et à mesure de leur parcours, constitue une bonne alternative. On calcule un score à partir des réponses données par le marcheur et au-delà d'une certaine valeur de score, la personne est considérée comme étant atteinte du MAM.
Il existe plusieurs types de questionnaires :- le questionnaire 'ESQ-III' ('Environmental Symptoms Questionnaire'), conçu par Sampson en 1983, comprend soixante-sept questions, portant sur les différents symptômes pouvant survenir en altitude (suite au MAM, à l'OPHA ou aux conditions environnementales). Utilisé dans de nombreuses études épidémiologiques et physiopathologiques sur le MAM et l'OPHA, au cours de ces dernières années, il a été reconnu comme un outil fiable 37,55.
- le questionnaire de Lake Louise, plus simple que l''ESQ-III', a été proposé en 1991. Il ne comporte que cinq questions sur les symptômes du MAM et une sixième question, subsidiaire, sur l'atteinte fonctionnelle du sujet causée par les symptômes. Il peut être complété par un bref examen clinique.
Des explications plus détaillées sur ces deux questionnaires se trouvent au chapitre 7 ('Méthode').
3.5.2 OPHA
Pour poser le diagnostic d'OPHA, on considère que l'étalon-or est une radiographie des poumons 37. Les champs pulmonaires sont alors divisés en quatre zones, avec le médiastin comme limite verticale et les hiles pulmonaires comme limite horizontale :
- Score = 0, si le parenchyme est normal
- Score = 1, si le parenchyme est douteux
- Score = 2, s'il y a un infiltrat interstitiel sur moins de 50% de l'ensemble des champs pulmonaires
- Score = 3, s'il y a un infiltrat interstitiel sur plus de 50% de l'ensemble des champs pulmonaires
- Score = 4, s'il y a un infiltrat alvéolaire
Un score supérieur à 1 pose le diagnostic d'OPHA.
Sur le terrain, le diagnostic clinique d'OPHA est posé lorsqu'on est en présence d'une cyanose, d'une tachypnée et de râles pulmonaires 37.
4. Physiologie et physiopathologie d'altitude
4.1 Alcalose respiratoire et compensation rénale
La première réaction d'adaptation de l'organisme à l'hypoxie est l'augmentation de la ventilation. Elle est proportionnelle au degré d'hypoxie et permet de maintenir aussi longtemps que possible la pression partielle d'oxygène dans le sang artériel (PaO2) dans les limites des valeurs que le sujet présente au niveau de la mer. A 5'800 mètres d'altitude, la ventilation au repos a déjà doublé. Néanmoins, à partir d'une certaine altitude, l'hyperventilation ne peut plus compenser complètement l'hypoxémie et le sujet le perçoit notamment par une nette diminution de sa capacité maximale d'effort. Déjà à 2'500 mètres, celle-ci est diminuée de 5 à 10%. Au sommet de l'Everest, où la PO2 inspirée est de 42,5mmHg, la consommation maximale d'oxygène (VO2max) est réduite à environ 1 litre par minute, ce qui correspond à 20-25% des valeurs rencontrées au niveau de la mer. Cette consommation équivaut à celle d'une marche lente 24 .
L'hyperventilation entraîne une baisse de la pression partielle de CO2 dans le sang artériel et, par conséquent, une alcalose respiratoire. L'augmentation du pH stimule alors l'excrétion rénale de bicarbonates, les reins cherchant ainsi à compenser l'alcalose par une acidose métabolique. Cette compensation rénale s'effectue lentement, sur plusieurs jours, d'où la nécessité d'une acclimatation, c'est à dire d'une montée progressive en altitude, qui laisse au corps le temps d'effectuer les modifications physiologiques nécessaires pour s'adapter à l'hypoxie. On sait en effet qu'une bonne acclimatation diminue le risque de survenue du mal aigu des montagnes 4,17,25,36,45 (cf. chapitre 5 'Acclimatation et prévention'). La compensation rénale de l'alcalose peut être complète jusqu'à environ 5'000 mètres. Au-delà, le pH reste alcalin et ce d'autant plus que l'altitude est plus élevée (entre 7.41 et 7.46 à 5'800 mètres, 7.47 à 6'300 mètres, 7.55 à 8'050 mètres, > 7.7 à 8'848 mètres) 25 .
4.2 Réponse de la ventilation à l'hypoxie (RVH)
La réponse de la ventilation à l'hypoxie correspond à l'augmentation de la ventilation qui fait suite à la chute de la pression partielle d'oxygène dans l'air inspiré. Elle survient dès que la pression partielle d'oxygène atmosphérique est inférieure à 100mmHg, ce qui correspond à une altitude d'environ 3'000 mètres. La pression partielle d'oxygène dans le sang artériel est alors d'environ 60mmHg et la saturation de l'hémoglobine en oxygène de 91%. Cette valeur est critique, car elle se trouve juste au début de la pente raide de la courbe de dissociation de l'hémoglobine et toute baisse supplémentaire de la PaO2 (par exemple, en cas d'affection des voies respiratoires, d'hypoventilation pendant le sommeil, de prise de sédatifs) entraîne une chute rapide de la saturation en oxygène 11.
L'intensité de la réponse ventilatoire à l'hypoxie est déterminée par la sensibilité des chémorécepteurs périphériques, sensibilité qui varie d'un individu à l'autre : pour une même baisse de la PIO2, certains répondront par une augmentation plus importante de la ventilation. La RVH est émoussée chez les habitants d'altitude et chez ceux qui ont vécu pendant plusieurs décennies en altitude. Les chémorécepteurs périphériques, sensibles à la baisse de la PaO2, se trouvent au niveau du glomus carotidien (juste au-dessus de la bifurcation de l'artère carotide commune). Ils effectuent la transmission d'un signal chimique en un signal électrique (stimulus neurologique) qui va stimuler les centres respiratoires bulbaires. On pense que la chémodétection de l'oxygène par les cellules glomiques carotidiennes s'effectue par l'intermédiaire de canaux potassiques sensibles à l'O2 26 . L'expérimentation animale a montré qu'une perte de l'innervation des corps carotidiens, suivie d'une exposition à l'hypoxie, entraînait une dépression respiratoire due à l'effet dépresseur central de l'hypoxie 27 . Les chémorécepteurs carotidiens sont sensibles à l'hypoxie, à l'hypercapnie, à l'acidose et aux agents chimiques qui interfèrent avec la phosphorylation oxydative 45,58.
Les chémorécepteurs centraux du tronc cérébral répondent, quant à eux, aux modifications du pH du liquide céphalo-rachidien (LCR). L'hypoxie, qui entraîne une augmentation de la fréquence respiratoire via les récepteurs carotidiens, est suivie d'une alcalose respiratoire avec augmentation du pH du LCR, augmentation qui pousse les récepteurs centraux à freiner la réponse ventilatoire, atténuant ainsi la tachypnée. L'acidose métabolique rénale et une modification du seuil de sensibilité des chémorécepteurs centraux et périphériques permettent néanmoins de poursuivre la stimulation ventilatoire. Il y aurait, en effet, une augmentation significative de la RVH après plusieurs jours en hypoxie 3.
Dans l'une de ses études, Richalet a montré que les sujets qui avaient la RVH la plus faible avaient plus de risque de développer un MAM ou un OPHA 45. D'autres auteurs ont fait la même constatation 4,30,44. Néanmoins, il semble que ceux qui ont atteint le sommet de l'Everest sans apport artificiel d'oxygène n'avaient pas toujours une RVH plus marquée que celle des sujets-contrôle 28 . A première vue en effet, une RVH vive, en maintenant la PAO2 aussi élevée que possible, devrait constituer une protection contre une hypoxie trop importante et donc contre le MAM. Cependant, la baisse de la PaCO2 qui entraîne une vasoconstriction cérébrale est aussi plus importante. Il s'ensuivrait une diminution plus marquée du flux sanguin cérébral que chez ceux qui ont une RVH faible et donc davantage de troubles des fonctions supérieures. D'ailleurs, les personnes qui vivent en altitude et dont on sait qu'elles sont moins susceptibles de souffrir du MAM, ont une RVH émoussée, peut-être suite à une adaptation tissulaire à l'hypoxie.
L'étude des fonctions pulmonaires en altitude, montre une augmentation du flux expiratoire de pointe dès qu'on se trouve à plus de 3'000 mètres, à cause de la diminution de la densité de l'air, sauf chez les sujets atteints d'un MAM sévère. Par contre la capacité vitale forcée et le MEF25 sont diminués (augmentation du volume sanguin pulmonaire, oedème interstitiel ?). Toutes ses valeurs reviennent aux valeurs initiales dès le retour au niveau de la mer. Un syndrome restrictif a été mis en évidence chez les sujets souffrant de mal chronique des montagnes 14.
4.3 Respiration périodique nocturne
Au niveau de la mer, la respiration périodique nocturne, qui se traduit par quelques épisodes d'apnée se greffant sur un rythme respiratoire régulier, survient habituellement au cours de la phase d'endormissement. En altitude, elle survient à n'importe quel moment du sommeil et d'autant plus fréquemment que l'altitude atteinte est plus élevée (elle occupe environ 24% du temps de sommeil à 2'440 mètres, 40% à 4'270 mètres et entre 57% et 90% à 6'300 mètres) 29 . Elle est plus ou moins marquée selon les individus. Non seulement elle perturbe le sommeil par des réveils fréquents, accompagnés de sensations de suffocation, mais elle entraîne également, après chaque phase d'apnée (qui dure environ huit secondes) 30 , une hypoxémie relativement importante sur des périodes courtes mais répétées : à 6'300 mètres, les sujets passent la moitié de leur temps de sommeil avec un taux de saturation de l'hémoglobine en oxygène qui n'est en moyenne que de 69% 31 . La durée d'un cycle de respiration périodique au niveau de la mer est de trente secondes. Elle raccourcit avec l'altitude : à 6'300 mètres, elle est de vingt secondes. Il y aurait une corrélation entre le nombre d'épisodes de respiration périodique nocturne, l'intensité de la RVH et une la susceptibilité à l'OPHA 32 .
L'acclimatation ne semble modifier ni l'incidence ni la durée des cycles de respiration périodique nocturne. Par contre, celle-ci est atténuée par la prise d'acétazolamide qui stimule les centres respiratoires, tandis que l'inhalation d'oxygène, pendant le sommeil, la fait disparaître 30.
4.4 Système cardio-vasculaire
4.4.1 Coeur
L'hypoxie stimule la fréquence cardiaque qui, au repos, augmente de façon linéaire avec l'altitude : elle passe, par exemple, de soixante battements par minute au niveau de la mer à 70/minute à 3'000 mètres et à 80/minute à 6'000 mètres. Par contre, à l'effort maximal, au-delà de 3'000-3'500 mètres, elle diminue progressivement avec l'altitude : pour une fréquence de 180/minute au niveau de la mer et jusqu'à 3'000 mètres, elle chute à 160/minute à 5'000 mètres et à 140/min à 7'000 mètres. Cela serait dû à une désensibilisation des récepteurs b-adrénergiques du myocarde suite à la stimulation sympathique persistante. Cette diminution de la fréquence cardiaque pourrait peut-être limiter les performances physiques en altitude, mais elle exerce aussi un effet cardioprotecteur en milieu hypoxique 33 .
L'apparition d'une polyglobulie de la lignée rouge, au bout de cinq à sept jours d'hypoxie chronique, joue aussi un rôle dans la diminution de la fréquence cardiaque (la fréquence cardiaque nécessaire pour accomplir un effort donné est inversement proportionnelle à l'hématocrite). Malgré ces modifications de fréquence, le débit cardiaque ne change pas. En effet, le volume d'éjection diminue, suite à une baisse des pressions de remplissages des ventricules gauche et droit, au fur et à mesure que l'altitude augmente (voir plus loin). Le rapport entre volume d'éjection et pression auriculaire droite reste constant, ce qui suggère que la contractilité myocardique est conservée malgré l'hypoxie. Même si celle-ci est extrême, les troubles du rythme cardiaque surviennent très rarement sur un myocarde sain. Par contre, une arythmie sinusale marquée est habituelle au cours de la respiration périodique nocturne.
4.4.2 Tensions artérielles systémique et pulmonaire
Il n'y a pas de modification significative de la tension artérielle systémique en altitude, tout au plus trouve-t-on parfois une augmentation de la pression systolique de l'ordre de 20mmHg. Il en va autrement de la circulation pulmonaire : on constate aussi bien chez les habitants de haute que de basse altitude, exposés de façon aiguë ou chronique à l'hypoxie, une hypertension artérielle pulmonaire (HTP) qui s'accentue encore à l'effort. Elle se développe suite à la vasoconstriction persistante des artérioles pulmonaires, engendrée par l'hypoxie. Cette réaction serait un vestige de la vie foetale où l'hypoxie relative (PaO2< 30mmHg), en entraînant la vasoconstriction des artères pulmonaires, permet de maintenir fermé le circuit de la circulation pulmonaire. A la naissance, l'arrivée massive d'oxygène dans les alvéoles fait chuter la vasoconstriction et permet à la circulation pulmonaire de s'établir. L'hypoxie d'altitude élève la pression artérielle pulmonaire en quelques minutes et celle-ci se stabilise en douze à vingt-quatre heures. A 4'500 mètres, sa valeur est le double de celle du niveau de la mer. Au bout d'une année passée à 4'540 mètres, l'augmentation de la pression artérielle pulmonaire au repos est de 12-18mmHg par rapport aux valeurs du niveau de la mer ; elle est encore plus importante à l'effort. L'inhalation d'oxygène fait disparaître la vasoconstriction pulmonaire seulement en cas d'hypoxie aiguë. Chez les habitants d'altitude et les personnes acclimatées, l'inhalation de ce gaz diminue le débit cardiaque et la pression artérielle pulmonaire, mais ne modifie pas la résistance vasculaire pulmonaire. Cependant, celle-ci devrait augmenter, suite à la chute de pression dans les capillaires pulmonaires, car alors leur recrutement diminue, de même que le diamètre de ceux qui restent ouverts. L'inhalation d'oxygène exerce donc son action dans ce cas aussi : au lieu d'augmenter, la résistance vasculaire pulmonaire reste stable. La persistance de cette résistance s'explique par le fait, qu'au bout de deux à trois semaines en altitude, surviennent des modifications structurelles des artères pulmonaires : leur paroi s'enrichit en cellules musculaires lisses. Le foetus présente lui aussi des artères pulmonaires particulièrement riches en cellules musculaires lisses, avec une hypertension artérielle pulmonaire, puisque cette artère communique avec la circulation systémique à travers le canal artériel. Ce nombre important de cellules musculaires lisses persiste chez les enfants nés en altitude, mais disparaît, après quelques semaines, chez les enfants nés au niveau de la mer. Ces changements structurels des parois vasculaires pulmonaires avec hypertension artérielle pulmonaire se rencontrent chez les habitants des Andes, mais pas chez les Tibétains. Ces derniers ne présentent pas d'hypertension artérielle pulmonaire, même à l'effort. Leur ethnie semble donc être particulièrement bien adaptée à l'altitude 39.
L'hypertension pulmonaire entraîne également une surcharge ventriculaire droite. Des électrocardiogrammes réalisés chez des personnes acclimatées ont montré une déviation axiale droite du complexe QRS (+107° à 8'800m), une augmentation de l'amplitude de l'onde P et des ondes T inversées ou aplaties dans les dérivations précordiales droites 34 .
4.5 Gradient alvéolo-artériel
Le gradient alvéolo-artériel d'oxygène, qui est la différence de pression partielle d'oxygène entre les alvéoles et le sang artériel systémique, est minime au niveau de la mer. Par contre, il augmente notablement en altitude et ce d'autant plus que l'altitude atteinte est plus élevée et que l'effort fourni est plus intense. Au sommet de l'Everest, il est de 6mmHg au repos et de 11mmHg à l'effort 35 . Ce gradient est inversement proportionnel à la capacité des diffusion de la barrière alvéolo-capillaire et c'est cette capacité qui diminue en altitude et à l'effort. En effet, elle dépend de :
- la différence de pression partielle d'oxygène entre les alvéoles et le sang capillaire. Celle-ci est diminuée en altitude, à cause de la baisse de la pression partielle d'oxygène dans l'air.
- du temps de transit des globules rouges dans les capillaires pulmonaires. Ce temps diminue à l'effort et l'équilibration entre oxygène alvéolaire et oxygène sanguin a moins le temps de se faire. En effet, la désaturation de l'oxyhémoglobine en altitude est bien plus marquée à l'effort.
- la distance de diffusion (épaisseur de la membrane alvéolo-capillaire). Il n'est pas rare d'ausculter en altitude, même chez les personnes asymptomatiques, des râles crépitants pulmonaires, révélateurs d'un oedème interstitiel débutant qui augmente la distance de diffusion.
- l'hypoxie d'altitude fait qu'on se déplace vers la partie raide de la courbe de dissociation de l'hémoglobine, spécialement au-delà de 6'000 mètres, et cela aussi est en défaveur de la diffusion de l'O2 des alvéoles vers le sang 36 .
Par contre, l'hypertension pulmonaire due à l'hypoxie d'altitude entraîne une diminution de l'inégalité ventilation-perfusion du territoire pulmonaire, due notamment à la gravitation et qui est en partie à l'origine du gradient alvéolo-artériel. Sutton a constaté que les patients qui avaient le MAM le plus sévère, quarante-huit heures après être arrivés en hélicoptère à 5'360 mètres, avaient également la PaO2 la plus basse (nette augmentation du gradient alvéolo-artériel), signant un perturbation importante des échanges gazeux au niveau pulmonaire 62.
4.6 Modifications hématologiques
4.6.1 Globules rouges
On peut déceler une augmentation de la concentration plasmatique d'érythropoïétine déjà après deux à trois heures d'hypoxie. Elle atteint un maximum en vingt-quatre à quarante-huit heures, puis diminue après trois semaines, pour atteindre finalement des valeurs non détectables. L'augmentation de l'hématocrite, significative seulement au-delà de 1'500 mètres d'altitude, est mesurable après cinq à sept jours. Cela permet aux personnes complètement acclimatées d'avoir, malgré l'hypoxie, la même quantité d'oxygène dans le sang qu'au niveau de la mer jusqu'à environ 5'300 mètres, alors que la saturation de l'hémoglobine en oxygène n'est, à cette altitude, que de 75% 37 . Cette augmentation de l'hématocrite offre donc une meilleure capacité de transport de l'oxygène, mais elle accroît aussi la viscosité sanguine et donc le risque de thrombose. La concentration d'hémoglobine augmente de façon exponentielle pour atteindre un plateau après environ six semaines à une altitude donnée. Ensuite, elle continue d'augmenter, mais parallèlement au volume plasmatique, donc sans modification de l'hématocrite. Pour 15g/dl au niveau de la mer, elle atteint environ 15,8g/dl après une semaine à 3'400 mètres, 17g/dl après deux semaines et 17,5g/dl après quatre semaines. A 5'400 mètres, elle atteint 20,5g/dl après quatre semaines et 23,7g/dl après huit semaines 38 . En général, ceux qui sont les plus performants au-dessus de 5'000 mètres ont une valeur d'hémoglobine d'environ 18g/dl : il s'agirait donc d'une valeur optimale d'adaptation à l'hypoxie. En effet, au-delà de 18g/dl d'hémoglobine, la viscosité du sang augmente rapidement, entraînant une augmentation de la résistance des circulations systémiques et pulmonaires et donc une chute du débit cardiaque 39 . Après un retour au niveau de la mer, l'hémoglobine retrouve ses valeurs de départ en six semaines environ.
Au-delà de 5'000 mètres, les reins ne parviennent plus à compenser complètement l'alcalose respiratoire, mais cela présente un avantage : en effet, la hausse du pH déplace la courbe de dissociation de l'oxyhémoglobine vers la gauche, ce qui augmente l'affinité de l'hémoglobine pour l'oxygène et facilite ainsi le passage de l'oxygène alvéolaire dans les globules rouges. Il a été démontré qu'à une telle altitude, où la capacité de diffusion de la barrière air-sang est diminuée, cela est préférable à une diminution de cette même affinité qui faciliterait le passage de l'oxygène du sang aux tissus 40 .
L'altitude entraîne également une augmentation du 2,3-diphosphoglycérate dans les globules rouges par activation d'enzymes de la glycolyse. Cela atténue l'augmentation de l'affinité de l'hémoglobine pour l'oxygène sans toutefois l'annuler complètement (déplacement de la courbe de dissociation vers la droite).
4.6.2 Plaquettes
La numération plaquettaire semble chuter (entre 3% et 26%) au cours des premiers jours en altitude. Elle augmenterait ensuite de 14% en 21 à 31 jours, pour revenir aux valeurs du niveau de la mer, au bout de 180 jours 41 . Les différentes études ne permettent pas encore de dire si l'altitude entraîne une modification de leur capacité d'adhésion. De même, la façon dont l'hypoxie affecte les facteurs de coagulation n'est pas encore claire. Il y a eu des cas de coagulation intravasculaire disséminée survenue dans le cadre d'un MAM ou d'un OPHA, mais celle-ci survenait trop tardivement pour pouvoir jouer un rôle causal et constituait donc plutôt une complication. Néanmoins, le risque thrombogène est nettement augmenté en altitude : augmentation de l'hématocrite, déshydratation, froid (vasoconstriction), éventuellement diminution de l'activité physique (le mauvais temps ou la fatigue obligent parfois à passer toute une journée dans son sac de couchage).
4.6.3 Médiateurs vasoactifs
Richalet a constaté que le stress hypoxique provoque une modification des concentrations plasmatiques des médiateurs vasoactifs dérivés de l'endothélium : l'augmentation des eicosanoïdes vasoconstricteurs (thromboxane et leucotriènes), prédominante au cours des deux premiers jours en hypoxie, est suivie d'une augmentation des eicosanoïdes vasodilatateurs (prostaglandines) au cours du deuxième et troisième jour. Les valeurs se normalisent au cours du huitième jour 46.
4.7 Déplacements liquidiens
L'altitude perturbe l'homéostasie des fluides et des électrolytes. Par exemple, malgré l'augmentation de l'osmolalité plasmatique due à la déshydratation, la concentration plasmatique de vasopressine n'est pas modifiée par rapport au niveau de la mer. On constate également un déplacement de l'eau corporelle du compartiment intracellulaire vers le compartiment extracellulaire (surtout l'espace interstitiel). Cependant, l'augmentation de l'hématocrite au cours des premiers jours en altitude est due à une diminution du volume plasmatique. Plusieurs facteurs sont en cause pour expliquer ce phénomène :
- la déshydratation, inévitable en altitude, même si les apports hydriques sont importants. En effet, elle survient facilement par rapport au niveau de la mer, notamment à cause de l'augmentation des pertes insensibles (augmentation de l'hyperventilation, associée à la sécheresse de l'air, et augmentation de la transpiration, due à l'effort).
- Le fait que, pendant la plus grande partie de la journée, le marcheur est en position verticale entraîne une augmentation de la pression hydrostatique dans les capillaires des membres inférieurs, ce qui facilite la sortie d'eau du compartiment vasculaire vers l'espace interstitiel.
- La compensation rénale de l'alcalose respiratoire entraîne une augmentation de la charge de bicarbonates au niveau du tube proximal du néphron, ce qui accroît aussi les pertes rénales de cations et d'eau. En fait, ce phénomène est plus marqué chez ceux qui ne souffrent pas de MAM et qui, par le maintien de leur diurèse, subissent une plus grande contraction de leur volume plasmatique. A plus de 4'000 mètres d'altitude, le volume plasmatique diminue d'environ 20% au cours des dix-huit premières semaines, puis remonte progressivement au cours des sept à quatorze semaines suivantes pour atteindre finalement une valeur inférieure d'environ 10% à celle du niveau de la mer 42 . Par contre, les sujets qui sont atteints du MAM tendent à avoir une antidiurèse, associée à une augmentation de leur volume plasmatique.
-
L'effort pourrait contribuer à cette augmentation du volume plasmatique chez ceux qui souffrent du MAM, via l'activation du système rénine-angiotensine-aldostérone. En effet, trois réponses physiologiques de l'organisme à l'effort peuvent renforcer les processus physiopathologiques du MAM et de l'OPHA :
- diminution de la saturation artérielle en oxygène
- rétention de sel et d'eau
- augmentation de la pression artérielle pulmonaire
Ces différents processus sont en effet tous plus marqués chez les personnes sujettes au MAM ou à l'OPHA 2. Il y aurait chez celles-ci une augmentation de l'aldostérone au repos et, à l'effort, une augmentation de l'aldostérone et de l'ADH. On ne sait pas encore s'il s'agit d'une conséquence de l'hypoxémie ou d'un désordre hormonal primaire. Les mécanismes de régulation du peptide atrial natriurétique, de la noradrénaline et des eicosanoïdes sont aussi perturbés dans le MAM 21.
Le tout se trouve résumé dans le tableau suivant (adapté de l'article de J.S. Milledge: Salt and Water control at altitude) 38 :
| Réponse physio-logique à l'altitude (pas de MAM) |
Réponse pathologique à l'altitude (MAM) |
Réponse physiologique à l'effort en basse altitude | |
| Volume urinaire | | ¯ | ¯ |
| Balance hydrique | Négative ? | positive ? | Positive ? |
| Excrétion de Na+ | | ¯ | ¯ |
| Volume plasmatique et liquide extracellulaire | ¯ | ? | |
| Aldostérone plasmatique | ¯ | | |
| ANP plasmatique | | - ? | |
| ANP : peptide atrial natriurétique | |||
4.8 Métabolisme
Etonnamment, la lactatémie des sujets acclimatés est basse, même à l'effort maximal et elle est d'autant plus basse que l'altitude atteinte est plus élevée. On pense que cela est dû notamment au fait que l'hypoxie chronique, via une baisse de la stimulation adrénergique, entraîne une diminution de la glycolyse et donc de la production de lactates. D'autre part, l'hypoxie est aussi à l'origine d'une réduction de la VO2max et donc d'une production moins importante de lactates 29.
4.9 Système nerveux central et oedème cérébral de haute altitude (OCHA)
Le système nerveux central est l'un des organes les plus sensibles à l'hypoxie. Il n'est donc pas étonnant que dans le MAM, les troubles neurologiques soient au premier plan. Les zones cérébrales qui semblent être les plus susceptibles de souffrir du manque d'oxygène sont la substance blanche, l'hippocampe, les tubercules quadrijumeaux supérieurs et les corps genouillés externes (région thalamique). L'hypoxémie est également à l'origine d'une vasodilatation cérébrale qui entraîne une augmentation de l'apport sanguin au cerveau. Celle-ci est en partie contrebalancée par la vasoconstriction cérébrale due à la chute de la PaCO2. Lassen a montré que cette augmentation du flux sanguin cérébral se maintient et même s'intensifie quelque peu après cinq jours passés à 3'800 mètres 31. Puis on observe une diminution au cours des jours qui suivent à la même altitude, due à l'augmentation de l'hématocrite.
Comme nous l'avons dit plus haut, dans certaines études, une RVH marquée paraît avoir un effet protecteur contre le MAM, tandis que, dans d'autres, elle apparaît plutôt comme un facteur de risque. L'hypothèse émise pour expliquer son effet protecteur est la suivante : le fait qu'avec une RVH marquée, la fréquence respiratoire augmente davantage entraîne une hypocapnie plus importante et donc une vasoconstriction suffisamment forte pour contrebalancer complètement la vasodilatation cérébrale hypoxique. Par contre, chez ceux qui ont une RVH plus faible avec des valeurs de PaCO2 proches de celles du niveau de la mer, la vasodilatation prédominante favoriserait la formation d'un oedème cérébral (voir plus loin). Une autre hypothèse est que la PaCO2 plus élevée et la PaO2 plus basse, associées à une RVH faible, entraîneraient une vasodilatation périphérique. Il s'ensuivrait une chute de la pression veineuse centrale avec diminution de la sécrétion du peptide atrial natriurétique (réglée par le degré de distension de l'oreillette droite) entraînant une antidiurèse dont on a vu plus haut qu'elle est corrélée avec une augmentation du volume plasmatique et une plus forte incidence du MAM.
Pour expliquer les cas où une RVH marquée semble être un facteur de risque, on a émis l'hypothèse suivante : la PaCO2 plus basse entraîne une vasoconstriction cérébrale plus importante, diminuant ainsi le flux sanguin cérébral. L'hypoxie cérébrale serait alors plus marquée, malgré le fait que la PaO2 est plus élevée que chez les sujets avec faible RVH.
L'oedème cérébral de haute altitude constitue la complication grave du mal aigu des montagnes. Si l'hypoxie met en route les processus physiopathologiques qui peuvent aboutir au MAM, elle ne constitue néanmoins pas la cause directe des symptômes, ceux-ci ne survenant que plusieurs heures après l'arrivée en altitude. Comme cela a déjà été dit plus haut, l'hypoxie entraîne une perturbation de l'homéostasie des fluides et des électrolytes corporels. L'augmentation du liquide extracellulaire serait notamment à l'origine des oedèmes périphériques fréquemment rencontrés en altitude. Elle pourrait également entraîner un léger oedème au niveau cérébral, correspondant aux symptômes précoces du MAM. Par contre, l'aggravation des symptômes, avec oedème cérébral franc, serait plutôt consécutive à la vasodilatation cérébrale hypoxique, dont nous avons parlé plus haut. Celle-ci ne peut, selon Lassen, être à l'origine des formes légères du MAM : en effet, la prise d'acétazolamide (Diamox®) ou une élévation modérée de la PaCO2 qui augmentent davantage le flux sanguin cérébral permettent néanmoins d'atténuer les céphalées d'un MAM léger 31. Mais cette vasodilatation pourrait être impliquée dans la pathogenèse du MAM sévère en générant un oedème cérébral de haute altitude. En effet, la vasodilation cérébrale ne permet plus à la tension artérielle de chuter au niveau artériolaire. Cela provoque une augmentation prolongée de la pression hydrostatique dans les capillaires cérébraux, entraînant des lésions de leur paroi. L'augmentation de la perméabilité de la barrière hémato-encéphalique qui s'ensuit aboutit à un oedème cérébral vasogénique 11. Mais comme tout le monde présente une vasodilatation en altitude sans forcément être malade, ça ne doit pas être le seul mécanisme en jeu. L'endothélium joue également un rôle très important comme régulateur de la perméabilité de la barrière hémato-encéphalique (influence de facteurs relâchés au niveau de l'interface cellules nerveuses-endothélium et dont la régulation pourrait être altérée par l'hypoxie).
On sait qu'un oedème vasogénique (extracellulaire, dû à une augmentation de la perméabilité de la barrière hémato-encéphalique) touche surtout la substance blanche (celle-ci, moins dense que la substance grise, est plus susceptible d'être envahie par du liquide d'oedème), alors qu'un oedème cytotoxique (intracellulaire, dû au gonflement des cellules) atteint autant la substance grise que la blanche. Une étude de Hackett a confirmé cette origine vasogénique de l'oedème cérébral de haute altitude : les IRM cérébrales effectuées chez neuf hommes atteints de cette pathologie montraient une nette atteinte de la substance blanche 21. Les anomalies les plus marquées se situaient au niveau du corps calleux. Une encéphalopathie anoxique consécutive à l'OPHA (concomitant chez huit des neuf patients) a pu être exclue du diagnostic différentiel par l'absence d'atteinte de la substance grise. Tous les patients ont récupéré sans séquelles (entre un jour et six semaines après l'épisode aigu). Deux d'entre eux, moyennement malades, avaient cependant des IRM normales. Hackett en a conclu que les images d'oedème vasogénique cérébral sont caractéristiques de l'OCHA, sans être toutefois indispensables au diagnostic. On sait qu'il y une légère augmentation du signal T2 dans la substance blanche, en cas de MAM, signal qui est intense en cas d'OCHA, ce qui parle bien pour un continuum entre ces deux maladies. On sait aussi que l'oedème vasogénique, contrairement à l'oedème cytotoxique, répond aux stéroïdes (qui diminuent la perméabilité de la barrière hémato-encéphalique).
Une méthode indirecte de mesure de la pression intracrânienne consistant à mesurer le déplacement de la membrane tympanique, a permis de mettre en évidence que les stades précoces du MAM ne sont pas liés à une augmentation de la pression intracrânienne, contrairement aux stades sévères 66. L'augmentation de la pression intracrânienne, corrélée à l'ampleur de l'oedème cérébral, est donc une caractéristique tardive du MAM qui manifeste alors une grande similitude de symptômes avec les autres maladies associées à une hypertension intracrânienne, par exemple les tumeurs cérébrales. La composition du liquide céphalo-rachidien n'est pas altérée, mais la pression dans le LCR est augmentée (27cmH2O chez une patiente évacuée pour perte de connaissance et cyanose, alors que la norme est de 15cmH2O ou 11,5mmHg). Les examens complémentaires de routine (FSC, chimie sanguine) ne montrent rien de particulier.
L'autopsie de malades décédés d'OCHA montre un cerveau oedématié, dont les circonvolutions sont tuméfiées et aplaties et les sillons comprimés. Il peut y avoir une herniation des amygdales cérébelleuses et de l'uncus. Il y a parfois une spongiose marquée, spécialement dans la substance blanche et des hémorragies pétéchiales. On a aussi trouvé des thromboses de sinus veineux survenues ante mortem et des hémorragies sous-arachnoïdiennes. Mais ces derniers cas ne constituent pas la règle.
4.10 Oedème pulmonaire de haute altitude (OPHA)
L'augmentation du liquide extracellulaire survenant en altitude, peut entraîner, en plus ou indépendamment des oedèmes périphériques et cérébral, un oedème pulmonaire interstitiel infraclinique. Mais l'évolution vers l'oedème pulmonaire de haute altitude avéré nécessite la mise en route d'autres mécanismes. En effet, bien que l'hypertension artérielle soit la règle en altitude, celle que développent les sujets qui souffrent d'OPHA est toujours plus importante que celle des sujets sains. Mais l'hypertension pulmonaire seule (par exemple, dans le cas d'une hypertension pulmonaire primaire) ne suffit pas non plus à provoquer un oedème pulmonaire, les artérioles pulmonaires parvenant malgré tout à faire chuter suffisamment la pression pour qu'elle soit à nouveau normale au niveau des capillaires. Hultgren a postulé que le fait que la vasoconstriction pulmonaire hypoxique n'est pas homogène à travers le territoire pulmonaire est en grande partie responsable du développement de
l'OPHA 27. En effet, la fermeture de certaines artérioles pulmonaires par vasoconstriction entraîne une hyperperfusion du reste des vaisseaux, avec transmission aux capillaires de ce territoire de la pression artérielle pulmonaire élevée. Il s'ensuit des dommages des parois capillaires avec extravasation de liquide et, finalement, de protéines et de globules rouges dans les alvéoles.
Les modifications hémodynamiques mises en évidence dans l'OPHA sont :
- élévation marquée de la pression artérielle pulmonaire
- pression artérielle pulmonaire bloquée normale
- résistance artériolaire (pré-capillaire) pulmonaire élevée
- en général, bas débit cardiaque
- désaturation artérielle sévère
Dans les cas plus graves, il se peut que la formation de thrombus dans les vaisseaux pulmonaires joue aussi un rôle. En effet, l'examen histologique est le même que celui qu'on retrouve en cas de syndrome de détresse respiratoire de l'adulte (SDRA), avec un oedème alvéolaire riche en protéines et des thrombus dans les petits vaisseaux 11.
Des études effectuées en laboratoire ont montré qu'une augmentation de la pression capillaire transmurale provoque des ruptures de la couche endothéliale capillaire et de la couche épithéliale alvéolaire. Il s'ensuit une exposition de la membrane basale qui, à cause de son importante charge électrique, serait en partie à l'origine de l'activation des leucocytes et des plaquettes. Ces lésions sont rapidement réversibles une fois que la pression capillaire transmurale chute, ce qui expliquerait la récupération clinique rapide après un retour en basse altitude 43 .
Steinacker a mesuré en laboratoire les valeurs hémodynamiques de treize sujets ayant déjà souffert d'OPHA 61. Il a constaté :
- une augmentation plus importante de la pression artérielle pulmonaire à l'effort, en normoxie et en hypoxie
- une plus grande inégalité du rapport ventilation-perfusion à l'effort, en hypoxie
- une capacité vitale inférieure de 10% à celle des sujets-témoins (ce qui équivaudrait à un lit vasculaire pulmonaire plus petit)
- une capacité résiduelle fonctionnelle moindre, déjà au repos
- 10% de volumes pulmonaires totaux en moins.
Tout cela suggère une différence intrinsèque de la compliance pulmonaire et de la composition du parenchyme et donc des différences possibles dans la capacité vasculaire pulmonaire. A l'effort, l'augmentation de la capacité pulmonaire de diffusion, du débit cardiaque, du volume d'éjection et de la fréquence respiratoire est aussi moins importante chez ceux qui ont déjà souffert d'OPHA. La moindre augmentation de la fréquence respiratoire est peut-être due à des volumes pulmonaires et à une compliance pulmonaire moins importants, mais surtout à une réponse ventilatoire à l'hypoxie (RVH) plus faible (qui apparaît donc dans cette étude comme un facteur de risque pour l'OPHA).
Cette variation des volumes pulmonaires pourrait donc être un reflet des variations de capacité et de résistance vasculaires (les sujets résistants à l'OPHA auraient un lit vasculaire pulmonaire moins riche en cellules musculaires lisses, diminuant ainsi le contenu tissulaire du poumon et en augmentant la compliance) ou bien, une différence intrinsèque au parenchyme lui-même qui, avec des volumes pulmonaires plus importants chez les sujets résistants à l'OPHA, diminuerait leur résistance vasculaire pulmonaire qui dépend notamment de ces volumes. L'hypertension pulmonaire peut parfois être suffisamment sévère chez les patients souffrant d'OPHA ou de mal des montagnes chronique ou subaigu pour entraîner une insuffisance cardiaque droite 42.
Les patients sans artère pulmonaire droite, avec hypoplasie d'une artère pulmonaire ou avec une restriction du lit vasculaire pulmonaire secondaire à une déformation de la cage thoracique sont plus à risque d'OPHA 27.
Hanaoka a trouvé une association significative entre la susceptibilité à l'OPHA et les facteurs génétiques HLA-DR6 et HLA-DQ4, de même qu'entre l'hypertension pulmonaire et HLA-DR6 22.
4.11 Catécholamines
L'hypoxie d'altitude entraîne une augmentation transitoire du taux sérique d'adrénaline et une augmentation plus durable du taux de noradrénaline. Hackett a montré qu'en effectuant un blocage a-adrénergique, par l'administration de mésylate de phentolamine (Régitine) à des patients avec OPHA, on diminue la pression artérielle pulmonaire et la résistance vasculaire pulmonaire 20. Cela entraîne une amélioration de la saturation artérielle en oxygène. L'effet est plus important que celui obtenu par l'inhalation d'oxygène, l'administration de nifédipine ou d'hydralazine (ces trois traitements font chuter la pression artérielle pulmonaire de 30% en moyenne). La vasoconstriction pulmonaire de l'OPHA serait donc en partie contrôlée par le système nerveux sympathique.
En effet, il arrive que certains patients, suite à un traumatisme crânien, développent un oedème pulmonaire, associé à des valeurs élevées de catécholamines plasmatiques. Cette évolution peut être empêchée par l'administration de b-bloqueurs. Cet oedème post-traumatique, comme l'OPHA, serait en partie dû à une surcharge de l'activité sympathique, d'où le succès de la phentolamine dans le traitement de l'OPHA.
4.12 Hémorragies rétiniennes en altitude
La prévalence de cette pathologie d'altitude varie beaucoup d'une étude à l'autre : Hackett a constaté qu'elle atteignait 4% des marcheurs à Pheriche (4'243m) 19. Vingt-trois pour cent de ceux qui ont été examinés présentaient également des râles pulmonaires, associés de manière significative au MAM, aux oedèmes périphériques et aux hémorragies rétiniennes. Par contre, Brunner a rencontré des hémorragies rétiniennes chez 56% des montagnards parvenus à 5'200 mètres 11. Ces hémorragies sont souvent multiples, en flammèche, accompagnées d'un engorgement artério-veineux, de foyers cotonneux et, parfois, d'un léger oedème papillaire. Le plus souvent, elles n'entraînent pas de symptômes (elles provoquent une vision floue si elles sont proches de la macula, rarement des scotomes) et disparaissent spontanément. Elles surviennent plus fréquemment au cours des premiers jours, et même si elles sont souvent associées à un MAM ou à des râles pulmonaires, on n'a pas mis en évidence de corrélation avec la sévérité du MAM. En effet, elles peuvent aussi toucher des personnes par ailleurs asymptomatiques. L'augmentation du flux sanguin cérébral due à l'hypoxie, associée à un accroissement soudain de la pression dans les vaisseaux rétiniens (Valsalva) pourrait entraîner des microruptures.
5. Acclimatation et prévention
5.1 Acclimatation
L'acclimatation consiste en une montée progressive en altitude. C'est le moyen le plus efficace de diminuer le risque de survenue du mal aigu des montagnes, sans pouvoir toutefois l'écarter totalement. En effet, plusieurs auteurs ont montré qu'au-delà de 2'500 mètres, le fait de ne pas dépasser 300 à 500 mètres de dénivelé entre deux nuits (on peut monter plus haut pendant la journée et ensuite redescendre pour dormir) diminue l'incidence du MAM et de l'OPHA 33,36. Au-delà de 4'000 mètres, les paliers devraient être idéalement de 150 mètres par jour pour que l'acclimatation soit optimale. Maggiorini a en effet constaté que l'incidence du MAM entre 2'850 et 4'560 mètres est inversement corrélée au nombre de nuitées préalablement passées à plus de 2'500 mètres 36 :
| Nuits à plus de 2'500 mètres | 0 à 3 nuits (n = 300) |
4 à 8 nuits (n = 75) |
9 à 12 nuits (n = 15) |
> ; 12 nuits (n = 31) |
| Incidence du MAM 44 | 75% | 68% | 53% | 42% |
| Score clinique moyen 45 | 1.75 ± 0.1 |
1.48 ± 0.2 |
1.2 ± 0.6* |
0.74 ± 0.2** |
| *p < ; 0.05, ** p < ; 0.01 (U-test) en comparant au groupe '0 à 3 nuits'; adapté de l'article de M. Maggiorini : Prophylaxe und Therapie der Höhenkrankheiten. 36 | ||||
Dans une étude effectuée en 1977, dans la région de l'Everest, Hackett a également constaté que, suite à une meilleure information sur le mal des montagnes, les marcheurs prenaient plus de temps pour s'acclimater et que, par rapport à l'étude qu'il avait effectuée en 1975, l'incidence du MAM avait chuté de 53% à 43% 18. La nécessité de l'acclimatation est aussi démontrée par le fait qu'une arrivée brutale à 6'000 mètres d'altitude entraîne une perte de connaissance et un coma, alors qu'une montée progressive sur plusieurs jours permet la plupart du temps d'y arriver sans encombre. Par contre, une descente rapide au niveau de la mer (par exemple en hélicoptère) est parfaitement tolérée par l'organisme.
Comme il a été dit plus haut, l'acclimatation laisse au corps le temps de mettre en route les mécanismes physiologiques qui le rendront apte à vivre en milieu hypoxique. Mais au-delà de 5'500 mètres, cette adaptation ne peut plus être complète et il faut beaucoup plus de temps pour qu'elle soit néanmoins maximale 33. Le transport de l'oxygène de l'air aux tissus passe par plusieurs étapes et, à chacune de celles-ci, une partie du précieux gaz est inévitablement perdue. Les modifications physiologiques dues à l'acclimatation tendent à atténuer ces pertes d'oxygène :
- l'air inspiré est humidifié lors de son passage dans les voies aériennes supérieures. La pression de vapeur d'eau à cet endroit est de 47mmHg (valeur constante, quelle que soit l'altitude), ce qui entraîne une chute de la PIO2 d'environ 10mmHg. L'effet de cette pression de vapeur d'eau joue un rôle encore plus important en altitude où la pression partielle d'oxygène dans l'air inspiré est diminuée par rapport au niveau de la mer.
- Au niveau de la mer, lors de son arrivée dans les alvéoles, la pression partielle d'oxygène chute de 50mmHg. Cette chute est due à l'addition de CO2 et au captage de l'oxygène par la circulation. Elle dépend en grande partie du degré du métabolisme et de la fréquence respiratoire. En effet, si la vitesse de la ventilation double, la chute de pression de l'oxygène alvéolaire est deux fois moins importante (c'est ce qui se passe à 5'800 mètres d'altitude). Au niveau de la mer, la pression alvéolaire d'oxygène est quasiment la même au repos et à l'effort, mais en altitude, l'augmentation de la fréquence respiratoire est comparativement plus importante à l'effort et la PAO2 est alors légèrement plus élevée qu'au repos.
-
Le passage de l'oxygène à travers la membrane alvéolo-capillaire entraîne une chute de sa pression de moins d'1mmHg au niveau de la mer. En altitude et au repos, le gradient alvéolo-artériel n'est que peu modifié jusqu'à environ 4'000 mètres, puis il augmente progressivement. Au sommet de l'Everest, ce gradient est d'environ 7mmHg : pour 35mmHg de PO2 alvéolaire, on a 28mmHg de PO2 dans les capillaires pulmonaires ! A l'effort, le gradient alvéolo-artériel augmente légèrement au niveau de la mer, mais il augmente de façon nettement plus marquée en altitude (il est de 13mmHg lors d'un effort maximal à 6'000 mètres) 46 . La diminution de la capacité de diffusion de l'oxygène est alors un des principaux facteurs limitant les performances physiques en altitude 47 . C'est une des étapes de perte d'oxygène sur laquelle l'acclimatation n'a pas d'influence.
Néanmoins, comme nous l'avons vu, l'altitude entraîne aussi une diminution de l'inégalité ventilation-perfusion à cause de la hausse de la pression artérielle pulmonaire, augmentant ainsi la surface pulmonaire à disposition pour les échanges gazeux. - La dernière étape est le passage de l'oxygène dans les tissus au niveau de la circulation capillaire, à l'origine du gradient artério-veineux, qui dépend du métabolisme, du débit cardiaque et de la concentration en hémoglobine. Comme nous l'avons dit, une modeste augmentation de l'hématocrite est suffisante, chez la personne acclimatée, pour compenser la réduction de la saturation de l'hémoglobine en oxygène, jusqu'à 5'300 mètres d'altitude. Néanmoins, cela se paie par une augmentation de la viscosité sanguine qui, si elle est trop importante, entraîne une diminution du débit cardiaque et donc de l'apport d'oxygène aux tissus.
Une expérience de Lyons a montré que le bénéfice de l'acclimatation persiste en tout cas huit jours lorsqu'on redescend au niveau de la mer : six sujets ont passé seize jours à 4'300 mètres, puis sont redescendus au niveau de la mer où ils sont restés pendant huit jours. Ils ont ensuite fait un retour simulé à 4'300 mètres, en chambre hypobare, pour une durée de trente heures. La fréquence du MAM était nettement moins élevée lors de la deuxième 'ascension' 34.
5.2 Acétazolamide (Diamox®®)
La prophylaxie du mal aigu des montagnes par l'administration orale d'acétazolamide a été démontrée dans plusieurs études 8,9,17,23,30,31,36. Ce médicament, en inhibant l'anhydrase carbonique, ralentit la réaction CO2 + H2OH+ + HCO3-. Au niveau du néphron, la sécrétion tubulaire des ions hydrogènes, de même que la réabsorption de bicarbonates et de sodium, sont alors diminuées. Il y aussi une augmentation de l'excrétion de potassium et l'élimination de tous ces ions favorise la diurèse aqueuse. L'augmentation de l'élimination des bicarbonates accélère donc la compensation rénale de l'alcalose respiratoire, facilitant ainsi le processus d'acclimatation. L'acétazolamide exerce aussi son action en stimulant les centres respiratoires 36. En effet, l'acidose métabolique qu'il entraîne provoque une augmentation du CO2 dans le liquide céphalo-rachidien. Une étude en double aveugle (acétazolamide/placebo) effectuée par Larson sur soixante-quatre grimpeurs ayant escaladé rapidement le Mont Rainier (4'394m) a montré que non seulement ceux qui étaient sous acétazolamide présentaient moins de symptômes dus au MAM, mais aussi que leur capacité vitale forcée et leur fréquence respiratoire augmentaient davantage en altitude (par diminution de l'oedème interstitiel ?) 30.
Ce médicament n'est néanmoins pas systématiquement recommandé comme moyen préventif, d'une part parce que le marcheur qui a pris le temps de s'acclimater ne sera pas forcément malade et d'autre part parce que, comme tout médicament, il comporte des effets secondaires : certains sont peu importants, telles les paresthésies des extrémités et une légère perte d'appétit. Par contre, la polyurie qu'il entraîne, oblige le marcheur à être d'autant plus attentif à boire abondamment pour éviter la déshydratation. D'autre part, l'acétazolamide, appartenant à la familles des sulfamidés, ne peut être administré aux personnes allergiques à ce type de médicament. De même, les patients asthmatiques, allergiques aux salicylés ou souffrant d'urticaire chronique peuvent présenter des réactions d'hypersensibilité cutanées et respiratoires dues au colorant contenu dans les capsules retard à 500mg.
La posologie recommandée pour la prophylaxie est de 250mg deux fois par jour ou de 500mg retard une fois par jour, en commençant vingt-quatre à quarante-huit heures avant le début de l'ascension. Le risque de survenue du MAM étant maximal durant les quatre ou cinq premiers jours en altitude, le traitement peut raisonnablement être arrêté au-delà.
6. Traitement du mal aigu des montagnes
Le degré d'agressivité du traitement dépend de la sévérité des symptômes. En effet,
la plupart des cas de MAM léger s'améliorent spontanément, en vingt-quatre à quarante-huit heures, si l'ascension n'est pas poursuivie. Un discret mal de tête pourra être soulagé par un comprimé de paracétamol ou d'acide acétylsalicylique (500mg ou 1000mg en une prise, respectivement jusqu'à six ou trois fois par jour). Si, malgré cela, les céphalées persistent, tout en restant légères, supportables, il convient de prendre un jour de repos ou plus, à la même altitude, pour permettre à l'organisme de s'acclimater. Il ne faut poursuivre l'ascension qu'après la disparition des symptômes, car le gain d'altitude entraînerait inévitablement une aggravation de ceux-ci, rendant alors la descente beaucoup plus pénible et difficile. Par contre, la descente doit être aussi immédiate que possible en cas d'aggravation des symptômes ou en cas de persistance de symptômes importants. Il faut descendre autant qu'il est nécessaire pour que ceux-ci disparaissent ou deviennent très légers. Souvent, une descente d'environ 500 mètres de dénivelé est suffisante, mais certaines personnes devront descendre davantage pour se sentir à nouveau bien. Si le déplacement est impossible, soit parce que le malade n'est pas en mesure de marcher seul et que personne n'est apte à le porter, soit parce que les conditions météorologiques sont trop difficiles et dangereuses, différents traitements d'appoint peuvent être prodigués en attendant :
- le caisson hyperbare. C'est un sac hermétique en polyamide dans lequel on couche le malade. Il est relié à une pompe qu'on actionne pour augmenter la pression de l'air à l'intérieur du sac. Le maintien de cette augmentation de pression, par environ dix coups de pompe par minute, simule une descente d'environ 2'000 mètres lorsqu'on se trouve à 4'000 ou 5'000 mètres. Le temps de recompression à l'intérieur du caisson dure entre une heure et cinq heures selon l'état du malade qui pourra ainsi redescendre dans de meilleures conditions.
- En cas de céphalées importantes ne répondant pas au paracétamol ou à l'aspirine, on peut essayer 400mg d'ibuprofène.
- La dexaméthasone, en diminuant la perméabilité de la barrière hémato-encéphalique, permet d'atténuer l'oedème cérébral et son cortège de symptômes. La dose de charge est de 8mg per os ou en intraveineux, suivie de 4mg toutes les six heures 36.
- L'acétazolamide peut également contribuer à atténuer les symptômes du MAM et à améliorer la PaO2. On recommande alors la dose de 250mg per os toutes les huit heures. On peut donc éventuellement s'en servir pour être soulagé de légers symptômes dus à l'altitude, sans pour autant que ces troubles soient suffisamment importants pour contraindre le marcheur à redescendre.
-
La nifédipine (Adalat®) est à administrer par voie orale, en cas d'OPHA. En 1989, Oelz a prouvé son efficacité pour diminuer la pression artérielle pulmonaire et entraîner une amélioration de l'oxygénation du sang, déjà quarante minutes après la première dose de nifédipine sublinguale 43. Au bout de quinze à trente minutes, le malade ressent une diminution de sa sensation de dyspnée et d'oppression thoracique. On constate aussi une diminution des symptômes du MAM, s'il est associé à l'OPHA, probablement suite à l'amélioration de l'oxygénation (diminution du gradient alvéolo-artériel durant les douze premières heures de traitement). Radiologiquement, on observe une disparition progressive des signes d'oedème alvéolaire déjà onze heures après le début du traitement. Tout cela a été observé malgré la poursuite de l'effort à plus de 4'000 mètres et sans apport artificiel d'oxygène. La prise de nifédipine n'a par contre pas entraîné dans ces cas de modifications significatives de la fréquence cardiaque et de la tension artérielle systémique 43. La dose initiale est de 10mg en comprimé sublingual ou de 20mgSR (comprimés 'retard'), suivie de 20mgSR toutes les six heures.
La nifédipine est également efficace comme prophylaxie de l'OPHA chez les sujets à risque (c'est-à-dire ayant déjà présenté un épisode d'OPHA), mais elle ne doit en aucun cas remplacer une bonne acclimatation.
L'inhalation d'oxygène est utile aussi bien en cas de MAM que d'oedème pulmonaire 1. S'il y en a suffisamment à disposition, commencer par 6-10 litres par minute au cours des premières heures, puis passer à 2-4 litres par minute, après amélioration de l'état du malade.
Nous rappelons qu'en aucun cas ces médicaments ne peuvent remplacer la descente qui est le seul remède curatif en cas de mal aigu des montagnes sévère. Ils n'ont qu'une fonction d'appoint en attendant que celle-ci puisse être réalisée ou pour la rendre plus aisée.
7. Méthode
7.1 Situation géographique
Au nord-ouest du Népal, au sein de l'immense chaîne himalayenne, se trouve le massif des Annapurnas. Il faut environ trois semaines pour parcourir à pied le tour de ce massif qui comprend plusieurs sommets culminant entre 7'000 et 8'000 mètres d'altitude. Ce tour des Annapurnas est un des treks les plus fréquentés du Népal. Il présente en effet de nombreux avantages : une variété impressionnante de paysages, une grande diversité de peuples et une montée progressive en altitude, permettant une bonne acclimatation. Il s'effectue en automne ou au printemps, car en hiver, la neige empêche le passage du col et, en été, les pluies abondantes de la mousson rendent les chemins impraticables.
Depuis Katmandou, il faut compter environ huit heures de bus pour arriver à Besisahar, point de départ du trek, à 823 mètres d'altitude. En effet, c'est là que la route goudronnée, qui s'étend chaque année un peu plus loin, se transforme en chemin de randonnée. Les marcheurs arrivent à Manang, à 3'535 mètres, pour la plupart après six jours de marche. C'est un village d'étape où l'on passe souvent deux nuits, pour mieux s'acclimater. C'est là aussi que se trouve l'un des deux dispensaires de l''Himalayan Rescue Association' (l'autre est à Pheriche, à 4'243 mètres, dans la région de l'Everest). Cette association, fondée dans les années septante par le médecin américain Peter Hackett, a pour but de favoriser la diffusion de l'information sur le MAM auprès des touristes, notamment à ces endroits stratégiques. En saison, elle emploie des médecins étrangers volontaires. Ils assurent chaque après-midi, au dispensaire, une conférence en anglais sur le mal aigu des montagnes. Ils sont également à disposition pour des consultations, aussi bien pour les touristes que pour les autochtones. Après Manang, il faut encore marcher deux jours (un jour pour certains) pour arriver à Thorong Phedi, à 4'500 mètres. C'est la dernière étape avant le passage du col de Thorong, point culminant du trek, à 5'416 mètres d'altitude. On se lève alors tôt le matin, pour arriver au col, après quatre à cinq heures de montée. Puis on redescend dans une autre vallée jusqu'au village de Muktinath, à 3'800 mètres d'altitude. Ensuite, il faut encore six jours de marche pour arriver à Beni où l'on retrouve une route carrossable. Ce parcours ne comporte aucune difficulté technique.
7.2 Questionnaires
Du 2 au 6 novembre 1998, cinq cents questionnaires portant sur les symptômes du MAM ont été distribués à Manang. Pour tenter d'inclure dans l'étude tous les touristes qui y ont séjourné au cours de cette période, la distribution des questionnaires avait lieu quotidiennement, d'une part au poste de l' 'Himalayan Rescue Association', après la conférence que donnait l'un des médecins de l'association, et d'autre part dans les quatorze lodges du village, au cours des repas de midi et du soir.
Les marcheurs étaient tenus de remplir les questionnaires chaque soir, à partir du dernier soir passé à Manang et jusqu'au soir suivant le passage du col de Thorong.


Les réponses données devaient correspondre aux symptômes ressentis au cours des vingt-quatre dernières heures. Le dernier soir de l'étude (correspondant au jour du passage du col), les questionnaires étaient remplis à Muktinath (3'800m), où ils étaient récoltés le lendemain matin.
Chaque questionnaire, rédigé en anglais, était composé de huit pages 48 . Les deux premières pages portaient sur des questions d'ordre général : date du jour, lieu d'hébergement, quantité de liquide absorbée pendant la journée, ainsi que les points suivants :
- caractéristiques personnelles (âge, sexe, état de santé, nationalité...)
- mode de vie (tabac, pratique d'un sport, expériences en altitude...)
- organisation du trek et équipement (grand ou petit groupe, vitesse de progression jusqu'à Manang...)
- connaissance du MAM (connaissance des symptômes, du traitement...)
La troisième page et suivantes comprenaient les deux questionnaires portant sur les symptômes du MAM : le questionnaire du score de 'Lake Louise' ('LLSS' pour 'Lake Louise Scoring System') et le questionnaire 'ESQ-III' (pour 'Environmental Symptoms Questionnaire' et 'III' car il résulte de la révision du questionnaire 'ESQ-II', lui-même issu du premier type de questionnaire 'ESQ' révisé).
7.2.1 Questionnaire et examen clinique de Lake Louise
Le questionnaire comprend six questions dont cinq portent sur les symptômes du MAM :
- céphalées
- troubles gastro-intestinaux
- fatigue et/ou faiblesse
- vertiges et/ou sensation d'étourdissement
- troubles du sommeil
La sixième question, à option, porte sur la répercussion desdits symptômes sur l'activité physique du marcheur (l'obligent-ils à diminuer voire à cesser son activité ?). Pour chacune des questions, le score le plus faible est de 0 (pas de symptômes et, pour la dernière question, absence de répercussion des symptômes sur l'activité physique) et le plus élevé est de 3 (symptômes sévères et, respectivement, sévère réduction de l'activité physique, contraignant au repos au lit). Le score du LLSS se calcule en additionnant les points de chacune des cinq premières questions : un score supérieur à quatre permet de poser le diagnostic de MAM 37.
Il peut être complété, si un médecin se trouve sur place, par un examen clinique ciblé qui examine :
- le status mental (1 point : léthargie, lassitude ; 2 points : désorientation, confusion ; 3 points : stupeur, diminution de l'état de conscience ; 4 points : coma)
-
la présence d'une ataxie, en effectuant le test de Romberg ou la marche sur une ligne droite, talon contre orteils (1 point : manoeuvres pour garder l'équilibre ;
2 points : ne parvient pas à marcher sur une ligne droite ; 3 points : chute ;
4 points : ne peut tenir debout) - la présence d'oedèmes périphériques (1 point : une localisation ; 2 points : plusieurs localisations)
Le score de Lake Louise global, correspondant au score du questionnaire additionné à celui de l'examen clinique, correspond au MAM s'il est supérieur à cinq.
7.2.2 'Environmental Symptoms Questionnaire-III' ('ESQ-III')
Ce questionnaire, défini par Sampson en 1983, comprend soixante-sept questions, au moyen desquelles on cherche à identifier différents symptômes pouvant survenir en altitude (notamment ceux liés au stress thermique, à la fatigue musculaire, au manque de sommeil...) 55. Vingt et une de ces questions portent spécifiquement sur le MAM. Elles distinguent les symptômes neurologiques (onze questions) et les symptômes respiratoires (douze questions), les questions se rapportant aux céphalées et aux nausées étant communes aux deux groupes de symptômes 49 . La quantification de la gravité des symptômes se fait entre 0 (absence de symptôme) et 5 (symptômes très sévères). Le chiffre de chaque réponse est ensuite multiplié par un poids factoriel spécifique au symptôme. Les résultats obtenus sont additionnés et cette somme est finalement divisée par 25.95, pour les questions relatives au MAM neurologique (abrégé 'AMS-C' pour 'Acute Mountain Sickness-Cerebral') et par 35.69 pour les questions du MAM respiratoire ('AMS-R' pour 'Acute Mountain Sickness-Respiratory'). La personne est considérée comme étant atteinte d'un MAM neurologique si son score 'AMS-C' est supérieur ou égal à 0.7 et d'un mal des montagnes respiratoire si son score 'AMS-R' est supérieur ou égal à 0.6.
Les onze symptômes retenus pour le calcul du MAM cérébral dans le questionnaire 'ESQ-III' sont :
- sensation d'étourdissement 50 (poids factoriel : 0.489)
- céphalées (0.465)
- vertiges (0.446)
- sensation de malaise 51 (0.346)
- vision floue (0.501)
- perte de coordination (0.519)
- faiblesse 52 (0.387)
- nausées (0.347)
- perte d'appétit (0.413)
- sensation d'être malade (0.692)
- sensation d'avoir la 'gueule de bois' 53 (0.584)
Formule de calcul du score AMS-C 54
AMS-C = X / 25.95
X = (C1 x .489) + (C2 x .465) + (C3 x .446) + (C4 x .346) + (C5 x .501) + (C6 x .519) + (C7 x .387) + (C8 x .347) + (C9 x .413) + (C10 x .692) + (C11 x .584)
Les douze symptômes relatifs au 'MAM respiratoire' sont :
- céphalées (0.312)
- souffle court (0.745)
- difficulté à respirer (dyspnée ; 0.763)
- respiration douloureuse (0.734)
- crampes d'estomac (0.516)
- douleurs dorsales (0.686)
- maux d'estomac (0.744)
- nausées (0.691)
- nez bouché (0.534)
- saignement de nez (0.578)
- insomnie (0.355)
- sensation d'être déprimé (0.480)
Formule de calcul du score AMS-R 55
AMS-R = Y / 35.69
Y = (R1 x .312) + (R2 x .745) + (R3 x .763) + (R4 x .734) + (R5 x .516) + (R6 x .686) + (R7 x .744) + (R8 x .691) + (R9 x .534) + (R10 x .578) + (R11 x .355) + (R12 x .481)
7.3 Examen clinique
Nous n'avons pas pu compléter le questionnaire de Lake Louise par l'examen clinique de ceux auxquels nous avons distribué les questionnaires. Il aurait fallu, pour ce faire, qu'un médecin soit présent à chaque étape pour examiner les marcheurs, juste avant ou après le moment où ils remplissaient le questionnaire. Néanmoins, nous voulions avoir une idée du score clinique de Lake Louise autour du col de Thorong. Quelques jours après avoir rejoint Muktinath, où mon collègue terminait la récolte des questionnaires, je suis donc repartie en direction du col de Thorong, afin d'examiner les marcheurs qui en descendaient ce jour-là. J'ai dû en croiser environ septante et j'en ai examiné une cinquantaine. Les huit premiers cas ont été examinés à 4'000 mètres d'altitude, les douze suivants à 4'300 mètres et enfin tous les autres à 4'600 mètres. Au cours de l'examen, qui durait moins de cinq minutes, j'ai fait une brève anamnèse pour savoir si le marcheurs présentait aussi des symptômes ou s'il en avait eu plus haut, lors du passage du col.
7.4 Méthode d'analyse statistique
Nous avons rentré toutes les données dans une base de données informatique. Nous avons évité le biais de sélection des données à ce moment-là, dans la mesure où c'était toujours la même personne qui dictait les résultats et l'autre qui les entrait dans l'ordinateur. Les données ont ensuite été analysées grâce au programme statistique SPSS (version 8.0). Le test de t de Student nous a permis de comparer les moyennes. Dans les cas où la distribution des données était anormale, nous avons utilisé le test non paramétrique de Mann-Whitney. La comparaison des proportions a été effectuée avec le test de c2 et l'analyse des tendances avec le test de c2 pour les tendances. La méthode de Pearson a été utilisée pour l'analyse de corrélations entre paramètres continus, tandis que la méthode de Spearman a servi à l'analyse de corrélations entre variables catégoriques. On a porté une attention particulière aux possibles facteurs de confusion : seuls les facteurs de risque réels, corrigés pour tous les paramètres de confusion, ont été rapportés.