Un seul gène peut dérégler le sommeil
Une équipe de l’UNIGE a identifié un gène essentiel dans la régulation des cycles veille/sommeil de la drosophile.
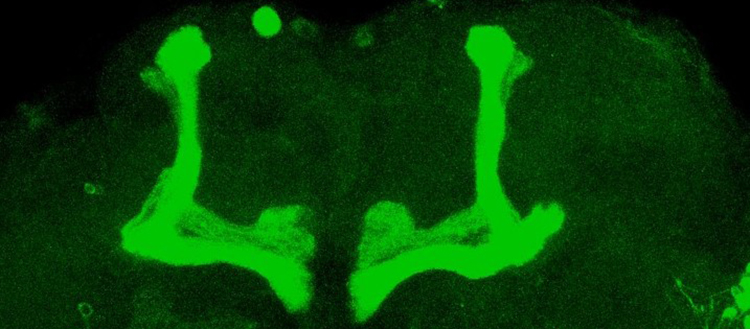
Les neurones du cerveau de la drosophile marqués par une protéine fluorescente verte. Les parties les plus colorées mettent en évidence les ‘mushroom bodies’, un centre clé de la régulation du sommeil. © UNIGE
Tous les organismes vivants sont soumis à un rythme biologique interne, qui contrôle de très nombreux processus physiologiques. Chez l’homme notamment, cette horloge interne suit un cycle de 24 heures et se manifeste même en l’absence de signaux déclencheurs externes, comme les changements de luminosité ou de température. En utilisant l’organisme génétique modèle Drosophila melanogaster, une équipe de l’Université de Genève (UNIGE) a découvert que le gène Nf1 est essentiel pour la régulation du cycle veille/sommeil. Ce gène est par ailleurs impliqué chez l’homme dans une maladie génétique fréquente – la neurofibromatose –, qui entraine la formation de tumeurs dans le système nerveux. Cette découverte pourrait aider à expliquer certains symptômes observés chez les patient-es atteinte-es de cette maladie, notamment le trouble de leur sommeil. Ces travaux sont à lire dans la revue Nature Communications.
La plupart des fonctions biologiques de l’organisme telles que le système veille/sommeil, la température corporelle, la fréquence cardiaque, la pression artérielle, la production d’hormones, mais aussi les capacités cognitives, l’humeur ou la mémoire sont régulées par le rythme circadien, un cycle d’une durée de 24 heures. C’est donc grâce à cette horloge interne, localisée chez l’humain au niveau de l’hypothalamus, que l’éveil est maximal du matin jusqu’en fin de journée, que la température corporelle est sensiblement plus élevée en journée ou encore que les contractions intestinales sont plus basses la nuit.
Toutes les espèces animales ou végétales ont leur propre rythme circadien et le laboratoire d’Emi Nagoshi, professeure au Département de génétique et évolution de la Faculté des Sciences de l’UNIGE, utilise la drosophile, cette petite ‘mouche du vinaigre’ que l’on trouve sur les fruits bien mûrs, pour étudier en détails les mécanismes de régulation de ces horloges internes. La drosophile est un modèle de choix pour la recherche en génétique: non seulement la mouche et son génome se manipulent très facilement en laboratoire, mais de très nombreux gènes sont conservés entre la mouche et les organismes supérieurs, ce qui permet souvent d’étendre le champ des découvertes de la mouche vers l’humain.
Veiller le sommeil des mouches
En utilisant des capteurs à infrarouge qui détectent les mouvements des mouches contenues dans des tubes, les scientifiques peuvent facilement analyser leurs cycles veille/sommeil. Sur une période de 24 heures, les mouches dorment environ 10 heures la nuit, puis sont actives toute la journée, à l’exception d’une sieste d’environ 4 à 5 heures. Les biologistes se sont intéressé-es à des mouches qui ont un cycle de sommeil déréglé et dont une zone particulière du cerveau, appelée corpora pedunculata (ou ‘mushroom bodies’ en anglais en raison de sa forme caractéristique), présente des lésions. Ils/elles ont ainsi analysé l’expression des gènes dans cette zone particulière du cerveau de drosophiles saines. «Nous avons identifié un gène, Nf1, dont l’expression fluctue en fonction des phases éveil/sommeil de la mouche: son expression augmente lorsque les mouches sont éveillées, alors qu’elle diminue pendant leur sommeil», explique Blanca Lago Solis, chercheuse dans le Département de génétique et évolution. Afin de confirmer le lien entre ce gène et le rythme circadien, les biologistes ont observé des mouches qui expriment faiblement ce gène, quel que soit le moment de la journée. «Ces mouches sont totalement déréglées et ont des phases de sommeil beaucoup plus nombreuses», rapporte la chercheuse genevoise.
Un lien potentiel avec la neurofibromatose
La protéine NF1 est en amont d’une cascade de régulation qui déclenche la libération de calcium, nécessaire à l’activation des neurones dans les ‘mushroom bodies’ du cerveau. L’expression de Nf1 en journée provoque donc une activité plus élevée des neurones de cette zone du cerveau le jour que la nuit, favorisant l’éveil diurne. L’homologue humain de Nf1 est un gène qui empêche le développement de tumeurs du système nerveux. «Lorsqu’une personne est porteuse d’une mutation dans le gène Nf1, elle est atteinte de neurofibromatose, une maladie génétique fréquente qui prédispose au développement de tumeurs du système nerveux. Un des symptômes des patient-es atteint-es de neurofibromatose est le dérèglement du sommeil et il sera intéressant d’explorer le rôle potentiel de Nf1 dans ce phénomène», conclut Emi Nagoshi.
